การเปลี่ยนแปลงครั้งใหญ่กำลังเกิดขึ้นในโรงพยาบาลไทยเมื่อระบบ Generative AI ถูกนำมาใช้สร้างบันทึกผู้ป่วยอัตโนมัติควบคู่กับระบบตรวจสอบทางการแพทย์ 'Clinical‑Guard' ที่ออกแบบมาเพื่อลดความผิดพลาดและยืนยันความถูกต้องเชิงคลินิก ในโครงการนำร่องที่กำลังเป็นที่จับตามอง พบว่าเวลาที่แพทย์ใช้ในการจดบันทึกลดลงเฉลี่ยราว 60% ทำให้แพทย์มีเวลาพบและดูแลผู้ป่วยเพิ่มขึ้นอย่างมีนัยสำคัญ ขณะเดียวกันองค์กรสุขภาพสามารถปรับปรุงคุณภาพข้อมูล เพิ่มความแม่นยำของรหัสวินิจฉัย และเร่งกระบวนการเรียกเก็บค่ารักษาพยาบาล
บทความนี้เป็นคู่มือเชิงปฏิบัติที่จะพาผู้อ่านผ่าน workflow การทำงานของ GenAI ในการสร้างบันทึกผู้ป่วย ตั้งแต่การเก็บข้อมูลจากการสนทนา การสรุปสังเขปอัตโนมัติ ไปจนถึงการตรวจสอบโดย 'Clinical‑Guard' พร้อมกรณีศึกษาจากโรงพยาบาลไทย ผลลัพธ์ที่วัดได้ และแนวปฏิบัติที่ดีที่สุดสำหรับการนำไปใช้จริงทั้งในประเด็นเทคนิค ด้านความปลอดภัยข้อมูล และการกำกับดูแล เพื่อให้ผู้บริหาร โรงพยาบาล และทีมไอทีมีแผนการปรับใช้ที่ชัดเจนและปลอดภัยต่อผู้ป่วย
บทนำ: เทคโนโลยี GenAI เข้าสู่ห้องตรวจไทยอย่างไร
โรงพยาบาลไทยเริ่มใช้ GenAI สร้างบันทึกผู้ป่วยอัตโนมัติ — ลดเวลาจดบันทึกของแพทย์เฉลี่ย 60%
การทดลองใช้งานในโรงพยาบาลต้นแบบของไทยรายงานผลชัดเจนว่าเทคโนโลยี Generative AI สามารถช่วยลดเวลาที่แพทย์ใช้ในการจดบันทึก ประวัติและสรุปการตรวจผู้ป่วยถึง 60% เมื่อเทียบกับกระบวนการบันทึกแบบดั้งเดิม โดยระบบนำเสียงบันทึกจากการตรวจจริงมาผ่านโมดูลสังเคราะห์ข้อความและสรุปผล ก่อนจะจัดวางข้อมูลให้อยู่ในฟิลด์ของระบบเวชระเบียนอิเล็กทรอนิกส์ (EHR) อย่างเป็นระบบ

แรงผลักดันสำคัญที่ทำให้โรงพยาบาลไทยให้ความสนใจเทคโนโลยี GenAI ได้แก่ ภาระงานของแพทย์ที่เพิ่มขึ้น การบันทึกข้อมูลทางการแพทย์ที่มีรายละเอียดจำนวนมาก และความต้องการปรับปรุงคุณภาพข้อมูลเพื่อการดูแลรักษาที่ปลอดภัยและมีประสิทธิภาพกว่าเดิม แพทย์ในหลายหน่วยงานรายงานว่าเวลาส่วนหนึ่งของการดูแลผู้ป่วยถูกใช้ไปกับงานเอกสารมากกว่าการสื่อสารกับผู้ป่วย ทำให้การนำ GenAI เข้ามาสนับสนุนสามารถตอบโจทย์ทั้งการลดภาระงานและเพิ่มเวลาให้แพทย์ได้ทำงานทางคลินิกมากขึ้น
ภาพรวมของโซลูชันที่โรงพยาบาลนำมาทดสอบประกอบด้วยสองโมดูลหลักคือ
- โมดูลสร้างบันทึกอัตโนมัติ (GenAI Note‑Generator): ประมวลผลเสียงหรือข้อความจากการสัมภาษณ์ผู้ป่วย สรุปอาการ ประวัติย่อ ผลการตรวจร่างกาย และข้อเสนอแนะเบื้องต้นในรูปแบบบันทึกที่พร้อมนำเข้า EHR ทั้งในรูปแบบข้อความยาวและฟิลด์โครงสร้าง
- โมดูลตรวจสอบทางการแพทย์ 'Clinical‑Guard': ทำหน้าที่ตรวจสอบความถูกต้องและความสอดคล้องของบันทึกทางคลินิก ใช้กฎทางการแพทย์ร่วมกับโมเดลการเรียนรู้เชิงลึกเพื่อตรวจสอบความขัดแย้ง เช่น ยาต้องห้ามต่อโรคประจำตัว ค่าห้องปฏิบัติการที่ผิดปกติที่ยังไม่ได้รับการลงความเห็น หรือข้อผิดพลาดทางการสะกด/หน่วยวัด พร้อมทั้งสร้างบันทึกการตรวจสอบ (audit trail) เพื่อให้แพทย์สามารถยืนยันหรือแก้ไขได้ก่อนบันทึกลงระบบถาวร
การผสมผสานระหว่างการสร้างบันทึกด้วย GenAI และการตรวจสอบด้วย Clinical‑Guard ช่วยให้ผลลัพธ์ไม่เพียงแต่ลดเวลาในการจดบันทึกเท่านั้น แต่ยังมุ่งเพิ่มความครบถ้วนของข้อมูล ลดความเสี่ยงจากข้อผิดพลาดเชิงเอกสาร และสนับสนุนการปฏิบัติตามมาตรฐานการรักษาในระบบโรงพยาบาล อย่างไรก็ตาม การนำไปใช้อย่างเต็มรูปแบบยังต้องคำนึงถึงการเชื่อมต่อกับ EHR นโยบายความเป็นส่วนตัว การมีมนุษย์เป็นผู้ยืนยันสุดท้าย และกระบวนการประเมินความปลอดภัยทางคลินิกก่อนการขยายสู่หน่วยงานอื่น ๆ
พื้นฐานเทคโนโลยี: GenAI สำหรับบันทึกทางการแพทย์ทำงานอย่างไร
พื้นฐานเทคโนโลยี: GenAI สำหรับบันทึกทางการแพทย์ทำงานอย่างไร
ระบบสร้างบันทึกทางการแพทย์ด้วย Generative AI (LLM) ทำงานเป็นสายการประมวลผลแบบเป็นทอด ๆ ที่ผสานหลายเทคโนโลยีเข้าด้วยกัน ตั้งแต่การแปลงเสียงเป็นข้อความ (speech-to-text) ไปจนถึงการเขียนกลับข้อมูลลงในระบบบันทึกสุขภาพอิเล็กทรอนิกส์ (EHR) โดยภาพรวมกระบวนการหลักประกอบด้วย 4 ขั้นตอนสำคัญ: การรับเสียงและแปลงเป็นข้อความ, การประมวลผลและสรุปด้วย LLM, การจับคู่เนื้อหากับแม่แบบ (template mapping) และการเขียนข้อมูลกลับสู่ EHR (write-back) ซึ่งระบบเชิงพาณิชย์ที่ดีสามารถลดเวลาจดบันทึกของแพทย์ได้มากถึง 60% ในเคสใช้งานจริง
- Speech-to-Text: ใช้โมดูลการรู้จำเสียง (ASR) ที่ผ่านการฝึกกับข้อมูลทางการแพทย์ เช่น คำศัพท์เฉพาะทาง ชื่อยา และคำย่อทางคลินิก เพื่อให้ได้อัตราความผิดพลาดต่ำสุด (typical WER ในระบบเฉพาะทางอยู่ในช่วง ประมาณ 5–15% ขึ้นกับคุณภาพเสียงและสำเนียงของผู้พูด)
- LLM สรุปและจัดโครงสร้าง: ข้อความที่ได้จะถูกส่งเข้า Large Language Model เพื่อสรุป แยกส่วนข้อมูลสำคัญ (เช่น อาการ, ประวัติ, การตรวจร่างกาย, แผนการรักษา) และแปลงให้อยู่ในรูปที่สอดคล้องกับมาตรฐานทางการแพทย์
- Template mapping: ข้อมูลสรุปจะถูกแมปลงแม่แบบทางคลินิก (SOAP, HPI, Assessment & Plan เป็นต้น) โดยใช้กฎการแมปและตัวชี้นำ (templates & field mapping) เพื่อให้ฟิลด์ข้อมูลตรงกับช่องใน EHR
- EHR write-back: ระบบจะเชื่อมต่อกับ EHR ผ่านมาตรฐานอินเทอร์เฟซ (เช่น HL7/FHIR API) เพื่อนำเข้าข้อมูลไปยังรีคอร์ดผู้ป่วย โดยมักมีชั้นอนุมัติจากผู้ใช้ก่อนการบันทึกขั้นสุดท้าย
ในเชิงเทคนิค การออกแบบ prompt และการปรับแต่งโมเดลมีบทบาทสำคัญต่อคุณภาพผลลัพธ์ Prompt engineering จะกำหนดกรอบ ให้ตัวอย่าง และข้อจำกัด (เช่น "สรุปเป็นหัวข้อสั้น ๆ ไม่เกิน 200 คำ ระบุสาเหตุที่เป็นไปได้ 3 ข้อ") เพื่อชี้นำ LLM ให้สังเคราะห์ข้อมูลตามรูปแบบที่ใช้งานจริง ส่วน fine-tuning จะใช้ชุดข้อมูลทางการแพทย์ภายในโรงพยาบาล (เช่น บันทึกผู้ป่วยที่ถูกอนุญาตและผ่านการทำให้ไม่ระบุตัวตนแล้ว) เพื่อฝึกโมเดลให้เข้าใจสไตล์ภาษาทางการแพทย์ท้องถิ่น คำย่อเฉพาะหน่วย และแนวปฏิบัติทางคลินิกของสถาบัน ผลจากการปรับแต่งมักเห็นเป็นการลดข้อผิดพลาดเชิงบริบทและเพิ่มความสอดคล้องกับแม่แบบเอกสาร
มาตรการด้านคุณภาพและการควบคุมมีความจำเป็นเพื่อให้ระบบปลอดภัยและเชื่อถือได้: การตรวจสอบแม่แบบ (template validation) ทำให้มั่นใจว่าฟิลด์สำคัญ (เช่น การวินิจฉัย, รายการยา, ขนาดยา) ถูกบันทึกครบถ้วนและอยู่ในรูปแบบที่ยอมรับได้ นอกจากนี้ระบบต้องออกแบบให้มี human-in-the-loop — แพทย์หรือนักสาธารณสุขตรวจสอบและอนุมัติก่อนบันทึกจริง ซึ่งช่วยจับข้อผิดพลาดเชิงความหมายและลดความเสี่ยงจากการสรุปที่ผิดพลาด ตัวอย่างการควบคุมอื่น ๆ ได้แก่บันทึกการเปลี่ยนแปลง (audit trail), การแจ้งเตือนความไม่สอดคล้องกับแนวทางคลินิก, และการทดสอบย้อนกลับ (retrospective auditing) เป็นระยะ
สุดท้าย การเชื่อมต่อกับระบบรอบข้างต้องคำนึงถึงความปลอดภัยและการปฏิบัติตามข้อกำหนด เช่น การเข้ารหัสข้อมูลในระหว่างส่ง (TLS), การจัดการสิทธิ์เข้าถึง, และการปฏิบัติตามกฎหมายคุ้มครองข้อมูลส่วนบุคคลของประเทศ ระบบที่ดีมักใช้มาตรฐานเชื่อมต่ออย่าง FHIR เพื่อให้การเขียนข้อมูลกลับ (write-back) เป็นไปอย่างราบรื่นและตรวจสอบได้ ในมุมธุรกิจ เทคโนโลยีเหล่านี้ไม่เพียงลดภาระงานเอกสาร แต่ยังเพิ่มประสิทธิภาพการดูแลผู้ป่วยและสนับสนุนการตัดสินใจทางคลินิกด้วยข้อมูลที่มีโครงสร้างและพร้อมใช้งาน
Workflow การทำงานของระบบและการรวมเข้ากับ EHR
Workflow การทำงานของระบบและการรวมเข้ากับ EHR
ระบบบันทึกผู้ป่วยอัตโนมัติที่นำ GenAI มาใช้ในโรงพยาบาลไทยถูกออกแบบให้ทำงานเป็นสายการทำงาน (workflow) แบบต่อเนื่อง ตั้งแต่การจับข้อมูลเสียงในห้องตรวจ ไปจนถึงการเขียนบันทึกลงในระบบ EHR โดยมีชั้นการตรวจสอบทางการแพทย์ของ Clinical‑Guard คั่นกลางเพื่อรับประกันความถูกต้องและความปลอดภัยเชิงคลินิก กระบวนการนี้เน้นหลัก human-in-the-loop โดยแพทย์ยังคงเป็นผู้อนุมัติขั้นสุดท้าย ระบบรองรับมาตรฐานการเชื่อมต่อ (เช่น FHIR/HL7) เพื่อให้การบันทึกสามารถผนวกเข้าสู่ EHR ได้อย่างราบรื่นและมี Audit Trail ที่ชัดเจน
ภาพรวมลำดับการทำงานแบ่งเป็น 4 ขั้นตอนหลัก ดังนี้:
- ขั้นตอน 1: รับเสียง/ข้อความจากห้องตรวจ (real-time capture) — ระบบจะสตรีมเสียงผู้ป่วยและแพทย์แบบเรียลไทม์หรืออัปโหลดไฟล์เสียงทันทีหลังการตรวจ ตัวแปลงเสียงเป็นข้อความ (ASR) จะทำการถอดความและเก็บ Metadata เช่น เวลา, หมอดูแล, ห้องตรวจ และบริบทการเยี่ยม ผู้ผลิตระบบรายงานว่า ASR แบบแพทย์เฉพาะทางมีความแม่นยำ >90% ในสภาพแวดล้อมคลินิกที่มีการฝึกสอนโมเดลเฉพาะภาษาท้องถิ่น
- ขั้นตอน 2: LLM สร้างร่างบันทึก พร้อมแทรกข้ออ้างอิงทางการแพทย์ — ข้อความที่ได้จะถูกส่งให้ LLM ที่ปรับแต่งด้วยข้อมูลทางการแพทย์ (fine-tuned) สร้างร่างบันทึกในรูปแบบ SOAP/OPD/H&P และแทรกข้ออ้างอิงเชิงหลักฐาน (เช่นการอ้างอิง PubMed ID, แนวทางการรักษาจาก WHO/NICE หรือรายการยาอ้างอิง) เพื่อให้แพทย์สามารถตรวจสอบแหล่งที่มาของคำแนะนำ ตัวอย่างการทำงาน: LLM สร้างสรุปอาการ, การวินิจฉัยเฉพาะที่เป็นไปได้, แผนการรักษา และเพิ่มบรรทัดอ้างอิงเช่น “(อ้างอิง: PubMed PMID: 12345678)” เมื่อจำเป็น
- ขั้นตอน 3: Clinical‑Guard ทำการตรวจสอบเชิงการแพทย์และปล่อยแจ้งเตือน — Draft จาก LLM จะถูกส่งผ่าน Clinical‑Guard ซึ่งประกอบด้วยกฎเหตุผลทางคลินิก, ตรวจสอบยา (drug‑interaction), การตรวจสอบค่าผลแลป ปริมาณยาผิดปกติ และการเปรียบเทียบกับแนวทางเวชปฏิบัติ หากพบความผิดปกติระบบจะสร้าง alert พร้อมคำอธิบายเชิงคลินิกและความร้ายแรง (low/medium/high) เพื่อให้แพทย์ทราบถึงประเด็นที่ต้องพิจารณา เช่น การเตือนการใช้ยาเกินขนาดหรือการขัดแย้งของยา
- ขั้นตอน 4: แพทย์ทบทวนและอนุมัติ ก่อนเขียนลง EHR — แพทย์จะได้รับร่างที่ผ่านการตรวจสอบพร้อมรายการแจ้งเตือน สามารถแก้ไข เพิ่มเติม หรือลบเนื้อหาได้แบบ WYSIWYG ก่อนกดอนุมัติ เมื่ออนุมัติแล้วระบบจะบันทึกบันทึกอย่างเป็นทางการลงใน EHR ผ่าน API ที่เข้ารหัสและบันทึกเวอร์ชันของเอกสารไว้สำหรับการตรวจสอบย้อนหลัง
ตัวอย่าง Sequence และเวลาที่ใช้ในแต่ละขั้นตอน (ตัวอย่างการใช้งานจริงจากการทดลองนำร่อง):
- 10:00–10:15 น. — การตรวจผู้ป่วย (10–15 นาที) พร้อมการสตรีมเสียงแบบเรียลไทม์
- 10:15:00–10:15:10 น. — ระบบ ASR ประมวลผลและส่งข้อความ (~5–10 วินาที)
- 10:15:10–10:15:40 น. — LLM สร้างร่างบันทึกโดยแทรกข้ออ้างอิง (20–30 วินาที)
- 10:15:40–10:15:55 น. — Clinical‑Guard รันการตรวจสอบเชิงการแพทย์และแจ้งเตือน (15–20 วินาที)
- 10:15:55–10:18:00 น. — แพทย์ทบทวน แก้ไข และอนุมัติ (เฉลี่ย 2–3 นาที; ลดจากเดิม 15–20 นาทีต่อเคส)
- 10:18:00–10:18:10 น. — บันทึกลง EHR และสร้าง Audit Trail (5–10 วินาที)
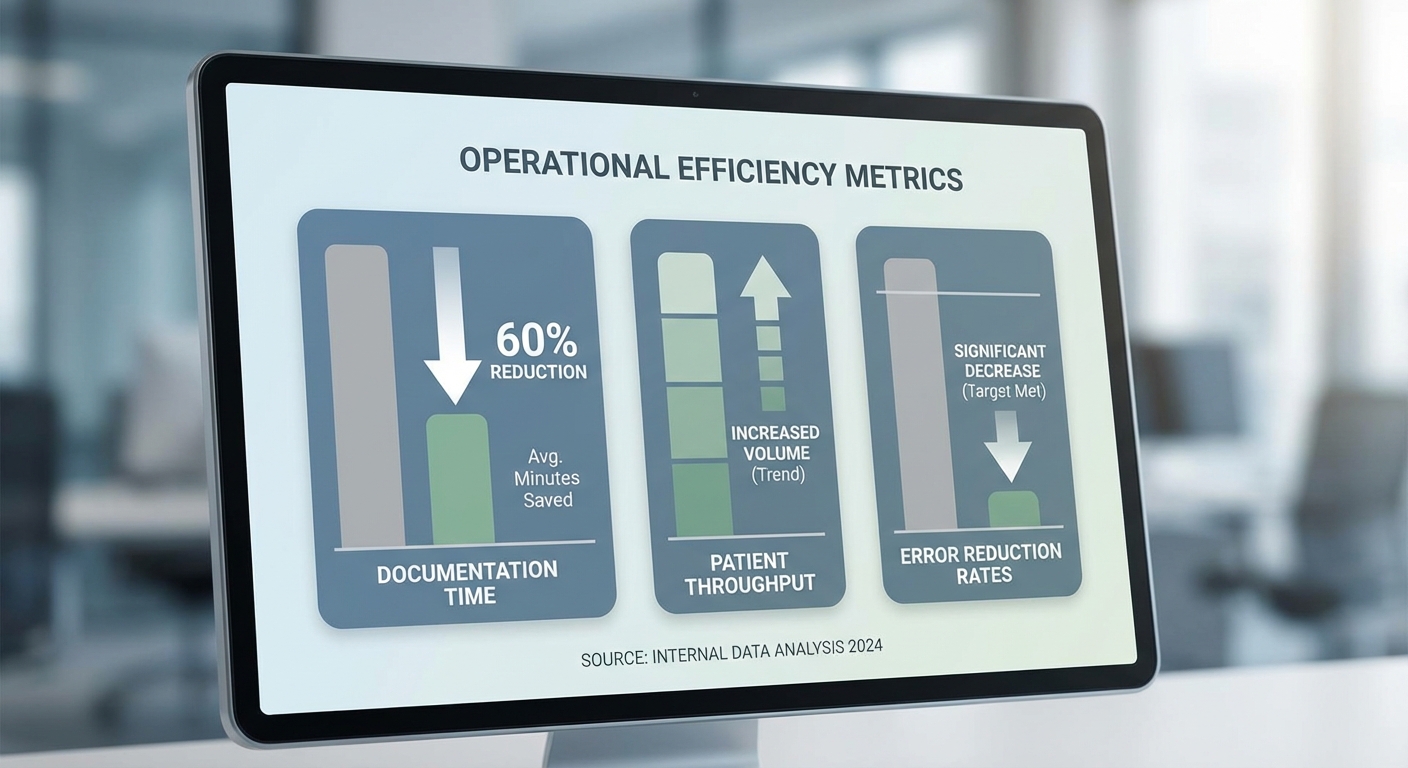
จากการนำร่องในโรงพยาบาลต้นแบบ พบว่าเวลาเฉลี่ยต่อการบันทึกลดจากประมาณ 20 นาทีต่อเคส เหลือ ~8 นาที (ลด ~60%) และระยะเวลาที่แพทย์ต้องใช้ในการแก้ไขร่างจาก LLM ลดลงเหลือเพียง 1–4 นาที ขณะที่ Clinical‑Guard ช่วยลดข้อผิดพลาดเชิงการแพทย์เบื้องต้น เช่น ความขัดแย้งของยา หรือการคำนวณขนาดยา ผู้นำระบบยังเน้นว่าแต่ละขั้นตอนต้องมีการบันทึกเหตุผลการแก้ไขของแพทย์เพื่อให้เป็นไปตามข้อกำหนดด้านกฎหมายและความปลอดภัยข้อมูล
ข้อควรระวังและการผนวกเข้ากับระบบ EHR: การรวมระบบต้องออกแบบการแมปข้อมูลระหว่างฟิลด์ของระบบบันทึกอัตโนมัติและโครงสร้างข้อมูลของ EHR (เช่น FHIR resources: Patient, Observation, MedicationRequest, Encounter) รวมถึงการจัดการสิทธิ์การเข้าถึง การเข้ารหัสข้อมูลขณะส่ง (TLS) และการเก็บ log/consent เพื่อให้สอดคล้องกับกฎหมายคุ้มครองข้อมูลสุขภาพ ระบบควรมีกลไกการย้อนกลับ (rollback) หากการบันทึกอัตโนมัติเกิดความผิดพลาด และต้องมีการเทรนนิ่งแพทย์ให้คุ้นเคยกับการทำงานร่วมกับร่างที่เกิดจาก AI เพื่อรักษาคุณภาพการดูแลผู้ป่วย
เจาะลึก: 'Clinical‑Guard' ฟีเจอร์และกลไกการตรวจสอบทางการแพทย์
เจาะลึก: ฟีเจอร์หลักของ Clinical‑Guard
Clinical‑Guard ถูกออกแบบมาเป็นเลเยอร์การตรวจสอบทางคลินิกที่ทำงานควบคู่กับระบบ GenAI ที่สร้างบันทึกผู้ป่วยอัตโนมัติ โดยมีเป้าหมายหลักคือเพิ่มความปลอดภัยของผู้ป่วยและลดภาระการตรวจทานของแพทย์ ฟีเจอร์สำคัญประกอบด้วย:
- Guideline adherence checks — ตรวจความสอดคล้องของแผนการรักษากับแนวทางมาตรฐาน (เช่น NICE, AHA, หรือแนวทางกรมการแพทย์) โดยระบบจะระบุจุดที่เบี่ยงเบนจากแนวทาง พร้อมอ้างอิงเอกสารทางคลินิก
- Drug‑check / Medication error detection — ตรวจการคำนวณขนาดยา, ความถี่, การให้ร่วมกันของยา (drug–drug interactions) และการทับซ้อนทางเภสัชกรรมที่อาจก่อให้เกิดความเสี่ยง
- Allergy alerts — แจ้งเตือนการสั่งยาที่ผู้ป่วยมีประวัติแพ้, รวมถึงการระบุตัวประกอบที่อาจก่อให้เกิดการแพ้ข้ามชนิด (cross‑reactivity)
- Contraindication checks — ตรวจเงื่อนไขห้ามใช้ยา/ห้ามใช้การรักษาตามประวัติผู้ป่วย เช่น ภาวะไตวาย ตับวาย หรือการตั้งครรภ์
กลไกการทำงาน: ผสมผสาน rule‑based, ML และเอกสารอ้างอิง
Clinical‑Guard ใช้วิธีการตรวจสอบแบบผสม (hybrid) เพื่อให้ครอบคลุมทั้งกฎที่ชัดเจนและการอนุมานเชิงบริบท:
- Rule‑based checks — กฎเชิงตรรกะสำหรับการคำนวณยา, ข้อห้ามพื้นฐาน และการจับคู่คำศัพท์จากบันทึก เช่น หาก eGFR <30 ให้เตือนลดขนาดยาโดยอัตโนมัติ
- ML‑based inference — โมเดลเรียนรู้เพื่อประเมินบริบทเชิงซ้อน เช่น การทำนายความเสี่ยงเลือดออกจากการใช้ยาหลายชนิด หรือการตรวจจับช่องว่างในประวัติที่บันทึกไม่ครบ เช่น อาการที่สำคัญถูกละเลย
- Linked clinical references — ทุกการเตือนจะถูกผูกกับแหล่งอ้างอิงทางคลินิก (guideline excerpt, journal summary) เพื่อให้แพทย์ตรวจสอบและตัดสินใจได้อย่างมีข้อมูลรองรับ
ระบบการให้คะแนนความเสี่ยงและการแทรกแซงแบบเรียลไทม์
เมื่อระบบวิเคราะห์บันทึกผู้ป่วย Clinical‑Guard จะคำนวณ Risk Score (ช่วง 0–100) จากการรวมค่าน้ำหนักของ rule hits, ผลการคาดการณ์ของ ML และความรุนแรงของความเบี่ยงเบนจาก guideline โดยกำหนดระดับความรุนแรง (severity) เป็น Low / Moderate / High / Critical เพื่อกำหนดวิธีการแจ้งเตือนและการแทรกแซง เช่น:
- Low (0–29) — แสดงเป็นไอคอน/ข้อความเล็กน้อยในบันทึก
- Moderate (30–59) — แสดง popup แนะนำการแก้ไขพร้อมปุ่มยอมรับการแก้ไขที่เสนอ
- High (60–84) — บังคับให้แพทย์ยืนยันหรือปฏิเสธ พร้อมบันทึกเหตุผล (audit trail)
- Critical (85–100) — แจ้งเตือนทันทีแบบ interruptive และแนะนำการดำเนินการฉุกเฉิน
การแทรกแซงแบบเรียลไทม์รวมถึงข้อเสนอการแก้ไข (suggested corrections) ที่คลิกเดียวเพื่อปรับรายการยา/ขนาดยา, template addendum สำหรับเติมข้อมูลที่ขาด, และตัวเลือกให้ส่งข้อความถึงเภสัชกรหรือทีมผู้ป่วยเฉียบพลัน ระบบยังมีการบันทึกการตัดสินใจของแพทย์เพื่อการตรวจสอบภายหลังและการปรับปรุงโมเดล
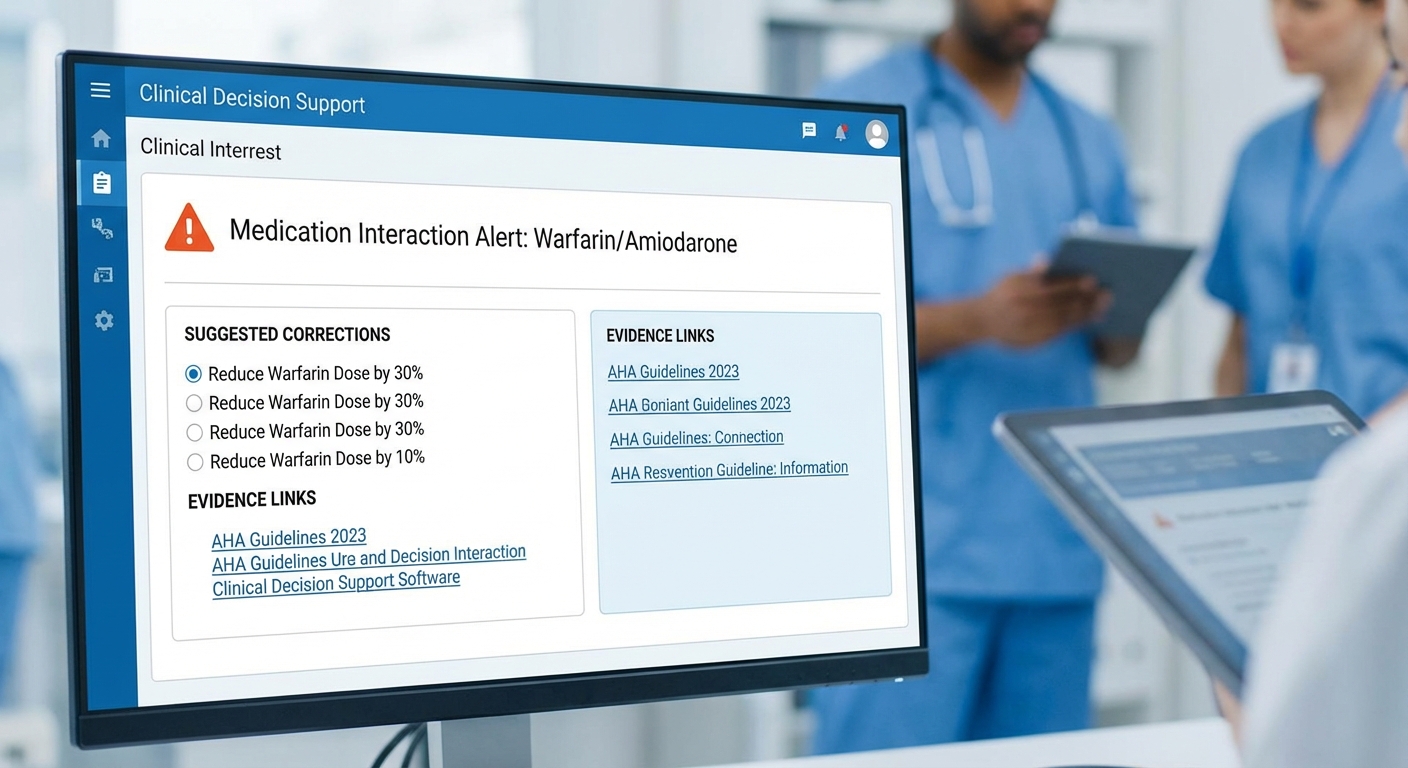
ตัวอย่าง alert และ mockup การแสดงผลใน UI
ตัวอย่างข้อความแจ้งเตือนที่อาจปรากฏในหน้าจอผู้ใช้:
- [Critical] High bleeding risk: Warfarin + NSAID detected. Suggested action: Hold ibuprofen; consult anticoagulation service. Evidence: AHA 2019 guideline; interaction severity high.
- [High] eGFR 22 mL/min — Reduce dose of Drug X from 500 mg → 250 mg. Evidence: Renal dosing table (hospital formulary).
- [Moderate] Missing allergy information — patient has prior documented penicillin anaphylaxis. Suggested action: Flag allergy on med list; replace with macrolide.
รูปแบบ UI mockup ที่ระบบนำเสนอจะเน้นความชัดเจนและความรวดเร็วในการตัดสินใจ: แผงแจ้งเตือนด้านขวาของหน้าจอบันทึก แบ่งตามระดับความรุนแรงด้วยสี (สีแดงสำหรับ Critical, ส้มสำหรับ High, เหลืองสำหรับ Moderate) แต่ละรายการแสดง ข้อความสรุป, Suggested correction, ปุ่ม Apply / Override พร้อมลิงก์ View evidence เพื่อเปิดคำอธิบายเชิงวิชาการหรือ excerpt ของ guideline
การทำงานร่วมกับผู้ใช้งานและการตรวจสอบความถูกต้อง
Clinical‑Guard ถูกออกแบบให้เป็นระบบ human‑in‑the‑loop ซึ่งหมายความว่าแพทย์เป็นผู้ตัดสินใจขั้นสุดท้าย ระบบสนับสนุนด้วยเหตุผลและหลักฐาน โดยมีฟีเจอร์สำคัญด้านการตรวจสอบความถูกต้อง ได้แก่ logging ของการตอบสนองต่อ alert, รายงานสรุปเชิงสถิติ (เช่น อัตราการยอมรับคำแนะนำ, false positive rate) และโมดูลปรับแต่งนโยบายเพื่อให้สอดคล้องกับแนวปฏิบัติของโรงพยาบาล
จากการทดสอบเบื้องต้นในสภาพคลินิกหลายแห่ง Clinical‑Guard รายงานตัวเลขเชิงบวก เช่น ลดข้อผิดพลาดยาได้ประมาณ 30–45% และช่วยลดเวลาจดบันทึกของแพทย์เฉลี่ย 60% เมื่อทำงานควบคู่กับ GenAI อย่างไรก็ตาม ระบบยังคงต้องการการตรวจสอบโดยมนุษย์และการปรับแต่งตามบริบททางคลินิกของแต่ละหน่วยงานเพื่อให้เกิดผลลัพธ์ที่ปลอดภัยและยั่งยืน
กรณีศึกษา: โรงพยาบาลไทยนำระบบไปใช้จริง ผลลัพธ์และบทเรียน
กรณีศึกษา: โรงพยาบาลไทยนำระบบไปใช้จริง ผลลัพธ์และบทเรียน
โรงพยาบาลระดับตติยภูมิแห่งหนึ่งในประเทศไทยได้ทำการทดสอบระบบ GenAI สร้างบันทึกผู้ป่วยอัตโนมัติควบคู่กับโมดูลตรวจสอบทางการแพทย์ “Clinical‑Guard” ในระยะเวลาพิสูจน์ความเป็นไปได้ 6 เดือน โดยครอบคลุมคลินิกผู้ป่วยนอกและหอผู้ป่วยในรวมประมาณ 12,000 encounter ผลการทดลองชี้ให้เห็นการเปลี่ยนแปลงทั้งเชิงปริมาณและเชิงคุณภาพที่ชัดเจน: เวลาจดบันทึกลด 60% ทำให้ทีมแพทย์สามารถเพิ่มเวลาปฏิบัติหน้าที่ต่อผู้ป่วยได้อย่างมีนัยสำคัญ เฉลี่ยแล้วโรงพยาบาลรายงานว่าเพิ่มเวลาเฉลี่ย 12 นาที/เคส สำหรับการสัมภาษณ์และการให้คำปรึกษาโดยตรงต่อผู้ป่วย
นอกจากเวลาจดบันทึกที่ลดลงแล้ว KPI สำคัญอื่น ๆ ยังแสดงผลเป็นบวก ได้แก่:
- ลดเอกสารซ้ำ: เอกสารซ้ำซ้อนระหว่างแผนกลดลงประมาณ 50% เนื่องจากระบบดึงข้อมูลจากฐานเดียวกันและสร้างบันทึกอ้างอิงได้อย่างสอดคล้อง
- ลดข้อผิดพลาดข้อมูลพื้นฐาน: ข้อผิดพลาดของข้อมูลประชากรพื้นฐาน (เช่น ชื่อ-นามสกุล, วันเกิด,ประวัติยาเดิม) ลดลง ~45% หลังนำระบบตรวจสอบอัตโนมัติของ Clinical‑Guard มาใช้
- ลดเวลารอผลรายงาน/สรุปการรักษา: เวลารอรับรายงานสรุป (discharge summary / specialist notes) ลดจากเฉลี่ย 24 ชั่วโมง เหลือประมาณ 7–8 ชั่วโมง
- คุณภาพบันทึกทางการแพทย์: การมี template และการตรวจสอบเชิงบริบทช่วยให้ความครบถ้วนของบันทึกเพิ่มขึ้นโดยการประเมินทางคลินิกภายในพบว่าความครบถ้วนของข้อมูลเพิ่มขึ้นจาก 72% เป็น 92%
ในด้านความคิดเห็นเชิงคุณภาพ ทีมแพทย์ให้ข้อคิดเห็นเช่น “ช่วยลดภาระการพิมพ์ข้อมูลหลังคลินิก ทำให้เรามีเวลาพูดคุยกับผู้ป่วยเชิงลึกมากขึ้น” แพทย์อาวุโสรายหนึ่งระบุว่า ระบบช่วยให้การสื่อสารแผนการรักษาชัดเจนและเป็นมาตรฐานมากขึ้น ในขณะที่พยาบาลรายงานว่าการส่งต่อข้อมูลระหว่างชั้นพยาบาลรวดเร็วขึ้นและคำถามซ้ำจากแพทย์ลดลง ผู้ป่วยจำนวนมากรายงานความพึงพอใจด้านเวลาในการได้รับคำอธิบายเกี่ยวกับแผนการรักษามากขึ้นและรู้สึกว่าผู้ให้บริการมีสมาธิมากขึ้นเมื่อทำการรักษา
อย่างไรก็ตาม ประเด็นที่ควรระวังและบทเรียนจากการนำระบบไปใช้จริงมีความสำคัญต่อการสเกลได้อย่างปลอดภัยและยั่งยืน:
- ต้องมีการฝึกอบรมแพทย์และบุคลากร: แม้ระบบจะช่วยอัตโนมัติ แต่การอ่านทวนและแก้ไขบันทึกทางการแพทย์เป็นสิ่งจำเป็น โรงพยาบาลจัดการอบรมเชิงปฏิบัติการ 3 ครั้งต่อกลุ่มงานและมีคู่มือการตรวจสอบเพื่อให้บุคลากรเข้าใจขอบเขตความรับผิดชอบ
- ปรับ prompt ให้เหมาะกับสำนวนภาษาท้องถิ่น: ระบบต้องปรับแต่ง prompt และ template ให้สอดคล้องกับสำนวนการสื่อสารทางการแพทย์ในภาษาไทยและแนวปฏิบัติของโรงพยาบาล การทดลอง A/B ในช่วงแรกช่วยลดความผิดพลาดทางความหมาย
- การมีมนุษย์เป็นผู้ตรวจสอบขั้นสุดท้าย (human‑in‑the‑loop): Clinical‑Guard ช่วยหาจุดผิดปกติแต่ไม่ควรแทนที่การตัดสินใจของแพทย์ ระบบออกแบบให้แพทย์ตรวจทานและยืนยันข้อมูลก่อนบันทึกขั้นสุดท้ายเพื่อลดความเสี่ยงด้านกฎหมายและความปลอดภัย
- การปรับตั้งค่าและเกณฑ์การแจ้งเตือน: โรงพยาบาลพบว่าต้องตั้งเกณฑ์ความไว/ความจำเพาะของการแจ้งเตือน Clinical‑Guard เพื่อหลีกเลี่ยง false‑positive มากเกินไป ซึ่งอาจสร้างภาระการตรวจสอบใหม่
- การปกป้องข้อมูลและการปฏิบัติตามกฎหมาย: ข้อกำชับด้านความเป็นส่วนตัวต้องได้รับการกำหนดชัดเจน ทั้งการเข้ารหัส การเข้าถึงตามบทบาท และการเก็บ log เพื่อการตรวจสอบย้อนหลัง
สรุปได้ว่า การนำ GenAI และระบบตรวจสอบทางคลินิกมาใช้จริงในบริบทของโรงพยาบาลไทยให้ผลลัพธ์เชิงบวกด้านประสิทธิภาพและคุณภาพการดูแลผู้ป่วย แต่ต้องมีการบริหารจัดการเชิงเปลี่ยนแปลง (change management) ฝึกอบรม ปรับจูนภาษาท้องถิ่น และกำกับดูแลด้านความปลอดภัย–จริยธรรมอย่างต่อเนื่องเพื่อให้การใช้งานยั่งยืนและปลอดภัยสำหรับผู้ป่วยและบุคลากรทางการแพทย์
ความเสี่ยง ด้านความเป็นส่วนตัว และข้อกำกับดูแล
ความเสี่ยง ด้านความเป็นส่วนตัว และข้อกำกับดูแล
การนำ Generative AI มาสร้างบันทึกผู้ป่วยอัตโนมัติในสถานพยาบาลไทยสร้างประโยชน์ด้านประสิทธิภาพ แต่ก่อให้เกิดความเสี่ยงด้านข้อมูลส่วนบุคคล (personal data / health data) ที่ต้องบริหารจัดการอย่างเข้มงวดตามกรอบกฎหมายและมาตรฐานทางการแพทย์ โดยเฉพาะ พระราชบัญญัติคุ้มครองข้อมูลส่วนบุคคล (PDPA) และแนวทางสาธารณสุขที่เทียบเคียงกับมาตรฐานระดับสากล (เช่น HIPAA-analogue) ซึ่งกำหนดหลักการเรื่องความยินยอม การจำกัดวัตถุประสงค์ การแจ้งเหตุละเมิดข้อมูล และสิทธิของเจ้าของข้อมูล เช่น สิทธิในการเข้าถึง แก้ไข และขอให้ลบข้อมูล
เชิงเทคนิคเพื่อบรรเทาความเสี่ยงต้องนำมาตรการหลายชั้นมาใช้ ได้แก่ การทำ de-identification/ anonymization โดยลบหรือแปลงตัวระบุโดยตรง (ชื่อ, เลขบัตรประชาชน, เบอร์ติดต่อ) และใช้เทคนิคเช่น pseudonymization, generalization ของวันที่, k-anonymity หรือการเติม noise ตามหลัก differential privacy เพื่อป้องกันการ re-identification นอกจากนี้ ควรใช้ on-premise processing หรือสถาปัตยกรรม hybrid ที่เก็บและประมวลผลข้อมูลจิตเวช/ข้อมูลผู้ป่วยในเครือข่ายของสถานพยาบาลก่อนจะส่งเฉพาะน้ำหนักโมเดลหรือฟีเจอร์ที่ไม่สามารถย้อนกลับมาเป็น PHI ได้ไปยังคลาวด์
นโยบายการจัดการความยินยอม (consent) และการเก็บข้อมูลเพื่อปรับปรุงโมเดลต้องชัดเจนและเป็นไปตาม PDPA — รวมถึงการบันทึกและพิสูจน์ความยินยอม (consent log), การให้ความยินยอมแบบละเอียด (granular consent) ว่าอนุญาตสำหรับการรักษา, การวิจัย หรือการใช้เพื่อฝึกโมเดล รวมทั้งกระบวนการจัดการการถอนความยินยอมและการลบข้อมูลตามคำขอ โดยหลักปฏิบัติที่แนะนำได้แก่:
- Data minimization: เก็บเฉพาะฟิลด์ที่จำเป็นต่อการวินิจฉัยหรือบันทึกทางคลินิกเท่านั้น และหลีกเลี่ยงการนำข้อมูลเสริมที่ไม่จำเป็นมาใช้ในการฝึกโมเดล
- Retention policy: กำหนดระยะเวลาการเก็บข้อมูลที่ชัดเจนตามวัตถุประสงค์ พร้อมกระบวนการลบข้อมูลอย่างปลอดภัย (secure delete) หลังหมดอายุหรือเมื่อเจ้าของข้อมูลขอถอน
- Alternatives to raw data storage: ใช้เทคนิคเช่น federated learning, synthetic data, หรือการฝึกด้วย differential privacy เพื่อลดการเก็บข้อมูลดิบ (raw PHI) ไว้ในศูนย์กลาง
การกำกับดูแลโมเดล (model governance) เป็นหัวใจสำคัญในการประกันความปลอดภัยและความรับผิดชอบ ต้องประกอบด้วย audit trail และการบันทึกกิจกรรมที่สามารถตรวจสอบได้ (who, what, when) สำหรับทั้งการเข้าถึงข้อมูลและคำสั่งเรียกใช้งานโมเดล รวมถึงระบบ versioning ของโมเดลและชุดข้อมูลฝึก (dataset lineage) เพื่อย้อนกลับและประเมินผลเมื่อเกิดปัญหา ตัวอย่างมาตรการที่ควรใช้ได้แก่:
- การเก็บ log ของ inference และการเปลี่ยนแปลงโมเดลพร้อม metadata เพื่อการตรวจสอบย้อนหลัง
- การทดสอบและ validation ทางคลินิกก่อนใช้งานจริง รวมทั้งการประเมิน bias และประสิทธิภาพแยกตามกลุ่มประชากร
- การกำหนด threshold ความเชื่อมั่น (confidence) ที่ต่ำกว่าระดับที่ยอมรับได้ให้ต้องมี human-in-the-loop ตรวจสอบหรือยืนยันผลลัพธ์
- การควบคุมการเข้าถึงด้วยบทบาท (RBAC), การเข้ารหัสข้อมูลทั้งขณะเก็บ (at rest) และขณะส่ง (in transit), และการตรวจสอบโดยหน่วยงานอิสระหรือการตรวจสอบภายในเป็นระยะ
สุดท้าย สถานพยาบาลควรจัดให้มีกระบวนการประเมินผลกระทบด้านคุ้มครองข้อมูล (DPIA/Data Protection Impact Assessment) ก่อนและหลังการนำระบบ GenAI ไปใช้จริง รวมทั้งแผนตอบสนองต่อเหตุละเมิดข้อมูล (incident response) ที่สอดคล้องกับ PDPA และแนวปฏิบัติของหน่วยงานสาธารณสุข เพื่อให้การลดภาระการจดบันทึกของแพทย์ (เช่น การลดเวลาได้ถึง 60%) เกิดขึ้นควบคู่กับการคุ้มครองสิทธิของผู้ป่วยและการปฏิบัติตามข้อกำกับดูแลอย่างครบถ้วน
คู่มือสั้น: ขั้นตอนการนำไปใช้จริงสำหรับโรงพยาบาล (Tutorial)
คู่มือสั้น: ขั้นตอนการนำไปใช้จริงสำหรับโรงพยาบาล (Tutorial)
การนำระบบ GenAI สร้างบันทึกผู้ป่วยอัตโนมัติ พร้อมระบบตรวจสอบทางการแพทย์ (เช่น “Clinical‑Guard”) เข้าสู่การปฏิบัติจริง จำเป็นต้องมีการวางแผนเชิงกลยุทธ์และการจัดการความเสี่ยงอย่างเป็นระบบ คู่มือนี้สรุปขั้นตอนปฏิบัติที่ชัดเจนสำหรับผู้ตัดสินใจในโรงพยาบาล ตั้งแต่การประเมินความพร้อม การเลือกพาร์ทเนอร์ การออกแบบ pilot การกำหนด KPI การฝึกอบรม ไปจนถึงแผนขยายการใช้งานแบบค่อยเป็นค่อยไป พร้อม checklist และตัวชี้วัดที่ควรติดตาม
ขั้นตอน 1: ประเมิน use-case และความพร้อมของ EHR
เริ่มจากการทำ inventory ของ use-case ที่มีมูลค่าทางคลินิกและธุรกิจสูง เช่น บันทึกผู้ป่วยนอก (OPD notes), สรุปการจำหน่าย (discharge summary), ED triage notes หรือบันทึกการเยี่ยมผู้ป่วยใน (ward rounds) ประเมินเวลาจดบันทึกปัจจุบันต่อเคส (ตัวอย่าง: 10–25 นาที/เคสในคลินิกนอก หรือ 20–45 นาที/เคสสำหรับการเยี่ยมผู้ป่วยใน) และคำนวณมูลค่าที่จะได้รับจากการลดเวลาการจดบันทึก (เช่น เป้าหมายลดเวลา 50–60%)
ตรวจสอบความพร้อมด้าน EHR/ระบบข้อมูล: รองรับมาตรฐานการแลกเปลี่ยนข้อมูล (FHIR/HL7), มี API สำหรับอินทิเกรชัน, รองรับ single sign‑on (SSO) และมีนโยบายการสำรอง/การเข้ารหัสข้อมูล หาก EHR ยังไม่พร้อม ให้จัดลำดับปรับปรุงก่อน pilot เช่น เปิด endpoint สำหรับ write-back ข้อมูลบันทึกและจัด schema mapping สำหรับข้อมูลที่ GenAI จะสร้าง
ขั้นตอน 2: เลือกพาร์ทเนอร์และกำหนด scope ของ pilot
เลือกพาร์ทเนอร์ด้าน GenAI และ Clinical‑Guard โดยพิจารณาจาก: ประสบการณ์ด้านสาธารณสุข, การรับรองด้านความปลอดภัยข้อมูล (เช่น HIPAA-equivalent, ISO27001), วิธียืนยันความถูกต้องทางการแพทย์ (clinical validation pipelines), และการสนับสนุนด้านเทคนิค (on‑prem vs cloud, SLA)
กำหนด scope ของ pilot ให้ชัดเจน: หน่วยงาน (ตัวอย่าง: คลินิกโรคหัวใจ หรือ ED), ขนาดตัวอย่าง (เช่น 200–500 encounter หรือ 4–8 สัปดาห์), โหมดการใช้งาน (shadow mode: ระบบรันเบื้องหลังแต่ไม่เขียนลง EHR; assistive mode: แสดงร่างให้แพทย์ตรวจและยืนยัน), ขอบเขตข้อมูลที่ให้ระบบเข้าถึง และแผนจัดการเหตุการณ์เมื่อพบข้อผิดพลาด
ขั้นตอน 3: ตั้ง KPI และตัวชี้วัดการวัดผล
กำหนด KPI ที่วัดผลได้และมีเป้าหมายเชิงตัวเลข ตัวอย่าง KPI หลัก:
- เวลาจดบันทึกเฉลี่ยต่อเคส — เป้าหมาย: ลดลงอย่างน้อย 50–60% จาก baseline
- ความถูกต้องของเนื้อหา (Clinical accuracy) — เป้าหมาย: ≥ 90–95% สำหรับข้อมูลโครงสร้างสำคัญ (diagnoses, medications, allergies)
- ความพึงพอใจของแพทย์ (Clinician satisfaction) — เป้าหมาย: คะแนนเฉลี่ย ≥ 4/5 ในแบบสำรวจหลังใช้งาน
- อัตราการแก้ไขโดยมนุษย์ — เป้าหมาย: ลดความจำเป็นในการแก้ไขร่างลงภายในช่วงที่ยอมรับได้ (เช่น แก้ไข < 20% ของบันทึก)
- ความปลอดภัยและเหตุการณ์ทางคลินิก — ไม่มีเหตุการณ์ความปลอดภัยสำคัญที่เกิดจากการใช้ระบบ (monitoring รายงานเหตุผิดพลาด)
- ความพร้อมใช้งานและ latency — SLA: uptime ≥ 99%, response time ≤ 2–5 วินาที ต่อการสร้างร่าง
กำหนดวิธีการวัด: ใช้ sampling audit โดยทีมแพทย์อาวุโส (เช่น random 5–10% ของบันทึก) และเครื่องมือเปรียบเทียบความแตกต่างเชิงเทคนิค (NLP similarity metrics, token-level F1 สำหรับข้อมูลโครงสร้าง)
ขั้นตอน 4: roll-out แบบค่อยเป็นค่อยไป พร้อม training และ feedback loop
ออกแบบการเปิดใช้งานแบบขั้นบันได (phased rollout):
- Phase A — Pilot (shadow mode): ระยะเวลา 4–8 สัปดาห์ เพื่อเก็บข้อมูล baseline และประเมิน accuracy โดยไม่กระทบ EHR
- Phase B — Controlled assistive: ให้แพทย์เห็นร่างและยืนยันก่อนบันทึกจริง ใช้งานในหน่วยงานที่เลือก 1–2 แผนกเพิ่มเติมเป็นเวลา 8–12 สัปดาห์
- Phase C — Expanded rollout: ขยายไปยังแผนกอื่นๆ พร้อม SOP และทีมสนับสนุน 24/7
การฝึกอบรมต้องเป็นแบบ role‑based: แพทย์ (การยืนยันร่าง, การตั้งค่าการสรุป), พยาบาล/เจ้าหน้าที่เวชระเบียน (การตรวจสอบข้อมูลโครงสร้าง), IT (การดูแลระบบ, logging), และทีมความปลอดภัยข้อมูล (compliance checklist) จัด simulation sessions, quick‑reference guides และ on‑demand knowledge base
สร้าง feedback loop ที่ชัดเจน: ให้มีช่องทางรายงานปัญหาแบบเรียลไทม์ (in‑app feedback), การประชุม weekly review ของคณะกรรมการคลินิก, และกลไก human‑in‑the‑loop เพื่อส่งตัวอย่างที่ระบบทำผิดกลับไปยังทีมพัฒนาสำหรับ retraining หรือ rule tuning
Checklist ก่อนเริ่ม pilot (สรุปเชิงปฏิบัติ)
- ระบุ use‑case ที่ชัดเจนและคำนวณ baseline เวลาจดบันทึก
- ตรวจสอบความพร้อมของ EHR: API, schema mapping, security
- เลือกพาร์ทเนอร์ที่มีประสบการณ์สาธารณสุขและรับรองความปลอดภัยข้อมูล
- กำหนด scope, ขนาดตัวอย่าง และระยะเวลา pilot
- ตั้ง KPI เชิงปริมาณและวิธีการวัด (sampling audit, surveys)
- เตรียมแผนการฝึกอบรมแบบ role‑based และ materials
- จัดตั้ง feedback loop และทีมรับผิดชอบการตอบสนอง
- เตรียมแผน rollback และ incident response สำหรับข้อผิดพลาดทางคลินิก
ตัวชี้วัดสำคัญที่ควรติดตามรายสัปดาห์/รายเดือน
- เวลาจดบันทึกเฉลี่ยต่อเคส (weekly)
- เปอร์เซ็นต์การลดเวลาเมื่อเทียบกับ baseline (monthly)
- ความถูกต้องของข้อมูลสำคัญ (diagnoses, medications) จากการตรวจสอบตัวอย่าง (weekly/monthly)
- คะแนนความพึงพอใจของผู้ใช้ (surveys หลังใช้งาน รายเดือน)
- จำนวนและความรุนแรงของ incident ทางคลินิกที่สัมพันธ์กับระบบ
- uptime, latency, และอัตราการตอบกลับของทีมซัพพอร์ต
- อัตราการแก้ไขร่างโดยผู้ใช้ (edit rate)
สรุป: การนำ GenAI และ Clinical‑Guard เข้าสู่การปฏิบัติจริงในโรงพยาบาลต้องดำเนินการอย่างเป็นขั้นตอน ตั้งแต่การประเมิน use‑case และความพร้อมของ EHR เลือกพาร์ทเนอร์ที่เชื่อถือได้ ออกแบบ pilot ด้วย KPI ที่ชัดเจน และขึ้นระบบด้วยการฝึกอบรมและ feedback loop ที่เข้มแข็ง เมื่อทำตาม checklist และติดตามตัวชี้วัดอย่างต่อเนื่อง โรงพยาบาลสามารถลดภาระเอกสารของแพทย์ได้อย่างปลอดภัยและมีประสิทธิภาพ พร้อมรองรับการขยายใช้งานในระยะยาว
บทสรุป
การผสานเทคโนโลยี Generative AI ในการสร้างบันทึกผู้ป่วยร่วมกับระบบตรวจสอบเชิงคลินิกอย่าง "Clinical‑Guard" แสดงผลชัดเจนว่า ช่วยลดภาระการจดบันทึกของแพทย์ได้ถึงประมาณ 60% และเสริมความปลอดภัยทางคลินิกด้วยการตรวจจับข้อผิดพลาดหรือความไม่สอดคล้องเบื้องต้นก่อนบันทึกลงในระบบ EHR อย่างไรก็ตาม การนำไปใช้ในวงกว้างต้องไม่ละเลยการควบคุมคุณภาพของข้อมูลและผลลัพธ์ เช่น การตรวจวัดความถูกต้องของบันทึก อัตราการยกเลิก/แก้ไขโดยแพทย์ (override rate) และอุบัติการณ์ความผิดพลาดทางคลินิก รวมทั้งมาตรการด้านความเป็นส่วนตัวของข้อมูลผู้ป่วยตามกฎหมาย (เช่น PDPA) และการรักษาความปลอดภัยข้อมูลด้วยการเข้ารหัส การควบคุมการเข้าถึง และบันทึกการตรวจสอบ (audit logs) เพื่อป้องกันความเสี่ยงด้านข้อมูลและคุ้มครองสิทธิผู้ป่วย
คำแนะนำสำหรับโรงพยาบาลคือเริ่มจากโครงการนำร่องที่มีขอบเขตชัดเจน กำหนด KPI ที่วัดผลได้ เช่น เป้าหมายลดเวลาเอกสาร (%) อัตราความถูกต้องของบันทึก อัตรการยอมรับจากแพทย์และผู้ป่วย เวลาในการแก้ไขข้อมูล และจำนวนเหตุการณ์ด้านความเป็นส่วนตัว พร้อมออกแบบกระบวนการ human‑in‑the‑loop ให้แพทย์/พยาบาลยังคงมีบทบาทตรวจสอบและให้ข้อเสนอแนะต่อเนื่องเพื่อปรับปรุงโมเดล มีมาตรการด้านข้อมูลและกรอบกฎหมายรองรับก่อนขยายผล และเตรียมแผนฝึกอบรมบุคลากร การติดตามเชิงปฏิบัติการ และกลไกทบทวนผลเพื่อตรวจจับเบี่ยงเบนหรือปัญหาเชิงคลินิกได้อย่างทันท่วงที ในอนาคตการรวม GenAI กับ Clinical‑Guard มีศักยภาพจะขยายไปสู่การสนับสนุนการตัดสินใจแบบเรียลไทม์ การวิเคราะห์แนวโน้มผู้ป่วยในระดับประชากร และการเชื่อมต่อระหว่างเครือข่ายสถานพยาบาล แต่ความสำเร็จระยะยาวขึ้นกับความเข้มแข็งของการกำกับดูแล ข้อกำหนดด้านจริยธรรม และการมีส่วนร่วมของบุคลากรทางการแพทย์อย่างต่อเนื่องก่อนการนำไปใช้ในวงกว้าง




