การมาถึงของปัญญาประดิษฐ์ (AI) ไม่ได้เป็นเพียงคำโฆษณาทางเทคโนโลยีอีกต่อไป แต่กำลังเปลี่ยนโฉมหน้าการดูแลสุขภาพอย่างเป็นรูปธรรม ตั้งแต่การช่วยวินิจฉัยภาพทางการแพทย์ที่แม่นยำขึ้น ระบบการเฝ้าระวังผู้ป่วยระยะไกลที่ต่อเนื่องไปจนถึงการออกแบบยาที่ใช้โมเดลเชิงคาดการณ์ การเติบโตของ AI ในวงการสุขภาพมีทั้งโอกาสและความท้าทายที่ซับซ้อน ภายในบทความนี้ เราจะชำแหละแนวโน้มหลักที่น่าจับตามองจนถึงปี 2034 พร้อมยกสถิติ แนวทางปฏิบัติ และตัวอย่างการนำไปใช้จริงเพื่อให้ผู้อ่านเห็นภาพชัดเจนว่าอนาคตของระบบสุขภาพจะเปลี่ยนไปอย่างไร
ผู้อ่านจะได้พบกับการวิเคราะห์แง่มุมสำคัญ ได้แก่ เทคโนโลยีที่เป็นหัวใจของการเปลี่ยนแปลง (เช่น การเรียนรู้เชิงลึก โมเดลสร้างสรรค์ และดิจิทัลทวินสำหรับโรงพยาบาล) กรณีศึกษาจากคลินิกและองค์กรที่นำ AI มาใช้จริง ผลกระทบต่อประสิทธิภาพ ค่าใช้จ่าย และการเข้าถึงบริการ รวมทั้งความเสี่ยงทางจริยธรรมและแนวทางกำกับดูแลที่จำเป็นเพื่อให้การนำ AI เข้าใช้เป็นไปอย่างปลอดภัยและยุติธรรม บทนำเชิงปฏิบัตินี้ตั้งใจให้ทั้งผู้กำหนดนโยบาย แพทย์ และผู้บริหารด้านสุขภาพได้รับมุมมองเชิงกลยุทธ์สำหรับการเตรียมพร้อมระยะยาวจนถึงปี 2034
บทนำ: ทำไม AI จึงเป็นตัวเปลี่ยนเกมในวงการสุขภาพ
บทนำ: ทำไม AI จึงเป็นตัวเปลี่ยนเกมในวงการสุขภาพ
ในสภาพแวดล้อมด้านสุขภาพปัจจุบัน ผู้ให้บริการและผู้กำหนดนโยบายต้องเผชิญกับความท้าทายเชิงระบบที่ซับซ้อน ได้แก่ ประชากรสูงวัยที่เพิ่มขึ้น ความต้องการบริการดูแลสุขภาพที่เพิ่มขึ้นควบคู่ไปกับ ต้นทุนที่พุ่งสูง และปริมาณข้อมูลทางการแพทย์ที่เติบโตอย่างรวดเร็วจากภาพรังสี เวชระเบียนอิเล็กทรอนิกส์ (EHR) จีโนมิกส์ และอุปกรณ์สวมใส่ ตัวอย่างเช่น หลายประเทศในกลุ่ม OECD มีสัดส่วนประชากรอายุ 65 ปีขึ้นไปมากกว่า 20% ซึ่งสร้างแรงกดดันด้านทรัพยากรบุคคลและงบประมาณ ขณะเดียวกันองค์กรสุขภาพต้องการการตัดสินใจที่รวดเร็วและแม่นยำขึ้นเพื่อปรับปรุงคุณภาพการรักษาและลดผลลัพธ์ที่ไม่พึงประสงค์

ปัจจัยเชิงระบบเหล่านี้ผลักดันให้เกิดการนำเทคโนโลยี AI มาใช้เป็นเครื่องมือสำคัญในการปรับโครงสร้างการให้บริการสุขภาพ โดยมีเหตุผลเชิงระบบสำคัญ 3 ประการที่ขับเคลื่อนการยอมรับอย่างกว้างขวาง:
- ข้อมูลปริมาณมาก: ข้อมูลทางการแพทย์ที่มีความหลากหลายและจำนวนมหาศาลจำเป็นต้องมีเทคโนโลยีที่สามารถประมวลผลและสกัดข้อมูลเชิงลึกได้อย่างมีประสิทธิภาพ
- ความต้องการประสิทธิภาพและความแม่นยำ: ระบบอัตโนมัติและโมเดลการเรียนรู้ของเครื่องสามารถลดเวลาการดำเนินงาน เพิ่มความแม่นยำในการวินิจฉัย และลดความคลาดเคลื่อนที่เกิดจากมนุษย์
- การขยายตัวของการแพทย์เฉพาะบุคคล: AI ช่วยผสานข้อมูลทางคลินิก จีโนมิกส์ และข้อมูลเชิงพฤติกรรม เพื่อสนับสนุนการวางแผนการรักษาที่เหมาะสมกับผู้ป่วยแต่ละคน
ในส่วนของการปฏิบัติทางคลินิก AI มีบทบาทโดดเด่นทั้งในการเพิ่มประสิทธิภาพการวินิจฉัยและสนับสนุนการตัดสินใจของแพทย์ ตัวอย่างเช่น ระบบวิเคราะห์ภาพด้วย deep learning ถูกนำไปใช้ในรังสีวิทยาและพยาธิวิทยาเพื่อช่วยตรวจจับความผิดปกติที่ยากต่อการมองเห็นด้วยตาเปล่า งานวิจัยและการใช้งานจริงชี้ให้เห็นว่า AI สามารถช่วยลดเวลาการอ่านภาพและกรองเคสที่ต้องการการดูแลเร่งด่วน ทำให้สามารถจัดลำดับความสำคัญผู้ป่วยได้ดียิ่งขึ้น นอกจากนี้ AI แบบพยากรณ์สามารถช่วยคาดการณ์ภาวะแทรกซ้อน เช่น การติดเชื้อในโรงพยาบาล (sepsis) หรือลดอัตราการกลับมารักษา (readmission) ทำให้การตัดสินใจทางคลินิกมีข้อมูลรองรับมากขึ้นและลดความเสี่ยงจากการตัดสินใจแบบอาศัยประสบการณ์เพียงอย่างเดียว
ในมุมมองตลาด แนวโน้มชี้ชัดว่าการลงทุนและงานวิจัยด้าน AI ทางการแพทย์กำลังเร่งตัวขึ้นอย่างต่อเนื่อง นักลงทุนสถาบันและบริษัทเทคโนโลยีเพิ่มงบประมาณด้าน R&D และสตาร์ทอัพด้านสุขภาพดิจิทัลได้รับการระดมทุนในระดับสูง รายงานเชิงอุตสาหกรรมคาดการณ์การเติบโตของตลาด AI ในสุขภาพที่มีอัตราการเติบโตเฉลี่ยต่อปี (CAGR) อยู่ในช่วงที่สูง (หลายสิบเปอร์เซ็นต์) ตลอดทศวรรษหน้า ขณะที่หน่วยงานกำกับดูแลและวงการวิชาการเริ่มอนุมัติและตีพิมพ์งานวิจัยที่สนับสนุนการใช้งานจริงมากขึ้น ซึ่งทั้งหมดนี้บ่งชี้ว่าภายในปี 2034 AI จะไม่เป็นเพียงเทคโนโลยีเสริม แต่จะกลายเป็นองค์ประกอบพื้นฐานของระบบการดูแลสุขภาพ
ผู้อ่านบทความนี้จะได้รับภาพรวมเชิงกลยุทธ์ของแรงผลักดันและโอกาสจาก AI ในภาคสุขภาพ ตลอดจนกรอบคิดสำหรับการประเมินความเสี่ยงและการลงทุนเชิงปฏิบัติ เพื่อให้ผู้บริหาร ผู้ลงทุน และผู้กำหนดนโยบายสามารถเตรียมกลยุทธ์ รับมือการเปลี่ยนแปลง และใช้ประโยชน์จาก AI อย่างมีประสิทธิภาพและยั่งยืนจนถึงปี 2034
เทคโนโลยีหลักที่ขับเคลื่อน AI ในสุขภาพ
เทคโนโลยีหลักที่ขับเคลื่อน AI ในสุขภาพ
การเติบโตของ AI ในภาคสุขภาพเกิดจากการผสานกันของหลายเทคโนโลยีหลักที่ตอบโจทย์ทั้งงานวินิจฉัย การติดตามผู้ป่วย และการสนับสนุนการตัดสินใจทางคลินิก โดยเทคโนโลยีเหล่านี้ไม่ได้ทำงานแยกส่วน แต่เชื่อมโยงกันผ่านการฝึกสอน การปรับใช้ และการประมวลผลข้อมูลเฉพาะทาง ในส่วนต่อไปจะลงรายละเอียดการทำงาน ประยุกต์ใช้ และตัวอย่างโมเดล/เฟรมเวิร์กที่เป็นที่ยอมรับในวงการ
Supervised และ Unsupervised / Self-supervised learning
พื้นฐานของโมเดลทางการแพทย์มักเริ่มจากการเรียนรู้แบบกำกับ (supervised learning) ซึ่งต้องการฉลากคุณภาพสูงจากผู้เชี่ยวชาญ เช่น แพทย์รังสีวิทยา หรือพยาธิวิทยา การเรียนรู้แบบไม่กำกับ (unsupervised) และ self-supervised learning ถูกนำมาใช้เพื่อแก้ปัญหาการขาดแคลนฉลาก โดยเรียนรู้ตัวแทน (representations) จากข้อมูลจำนวนมาก เช่น การใช้วิธี contrastive learning (SimCLR, MoCo) หรือ masked image/text modeling เพื่อ pretrain แล้วจึง fine-tune กับข้อมูลมีฉลาก ผลลัพธ์ในงานวิจัยชี้ว่า pretraining ด้วยวิธี self-supervised มักช่วยเพิ่มความแม่นยำของงาน downstream 5–15% ในชุดข้อมูลทางการแพทย์ที่มีขนาดจำกัด
Deep learning สำหรับภาพรังสีและพยาธิวิทยา
ในเชิงภาพ (medical imaging) เทคโนโลยีที่โดดเด่นคือ convolutional neural networks (CNNs) และสถาปัตยกรรม Transformer ที่ปรับมาใช้กับภาพ (Vision Transformers) ซึ่งได้รับการพิสูจน์แล้วว่าใช้งานได้ดีทั้งในภาพรังสีทั่วไปและสไลด์พยาธิวิทยา ตัวอย่างโมเดลที่ใช้บ่อยได้แก่ ResNet, DenseNet, EfficientNet ในกลุ่ม CNN และ ViT, Swin Transformer ในกลุ่ม Vision Transformer
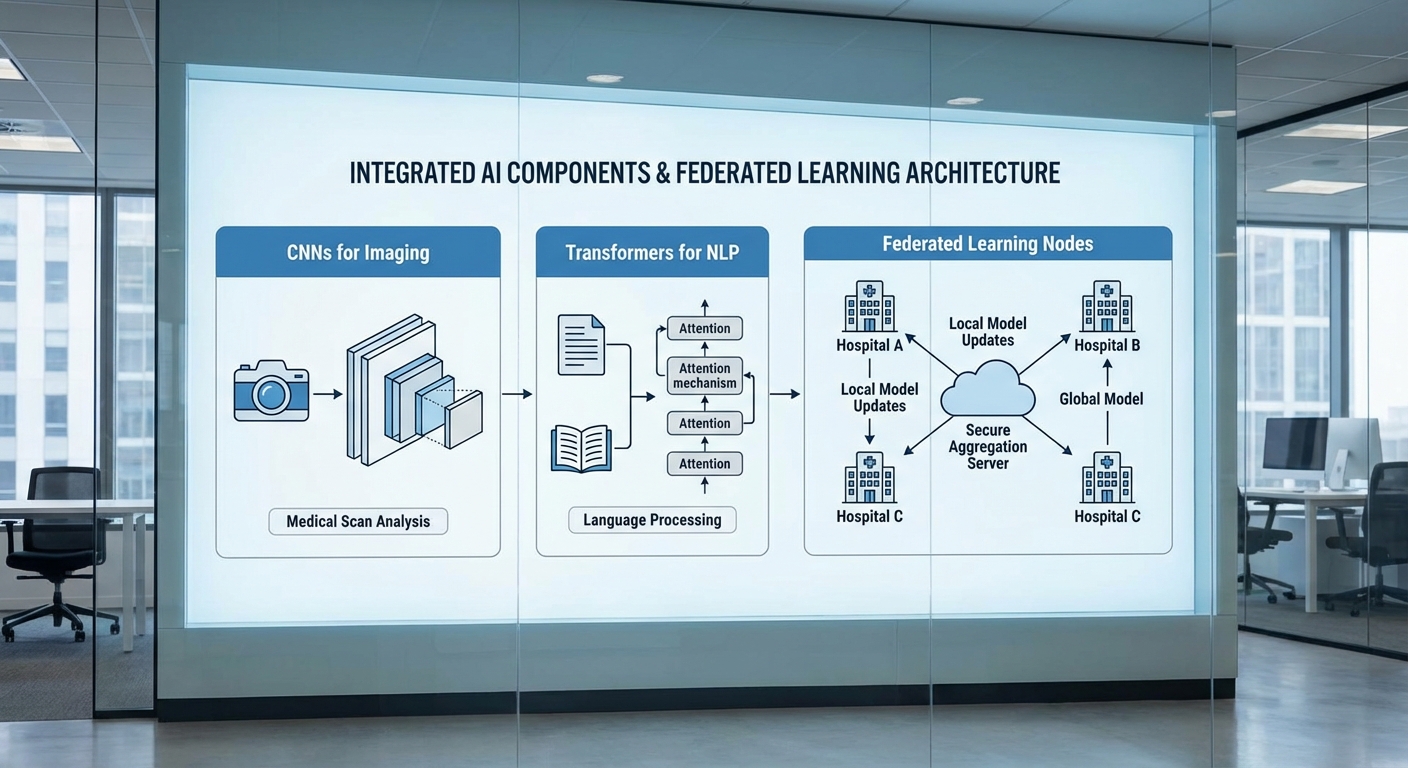
- การประยุกต์ทางคลินิก: ตรวจคัดกรองมะเร็งปอด/เต้านมจาก CT/Mammo, ตรวจหาเลือดออกในสมองจาก CT แบบเร่งด่วน, segmentation ของเนื้องอกและการวัดขนาดใน MRI, การวิเคราะห์สไลด์พยาธิวิทยาเพื่อหามะเร็งเซลล์มะเร็ง เป็นต้น
- วิธีการเชิงปฏิบัติ: ใช้ transfer learning จากโมเดลที่ pretrained บน ImageNet หรือ medical datasets, ใช้ patch-based training และ multiple-instance learning สำหรับสไลด์ขนาดใหญ่, และนำ attention mechanism มาช่วยตีความจุดสำคัญในภาพ
- ผลลัพธ์เชิงประสิทธิภาพ: งานวิจัยหลายชิ้นแสดงว่าโมเดล DL บางรุ่นสามารถใกล้เคียงหรือเกินประสิทธิภาพของผู้เชี่ยวชาญในงานเฉพาะ เช่น การตรวจหาเนื้องอกขนาดเล็กหรือการคัดกรองเบื้องต้น อย่างไรก็ตามปัจจัยด้านชุดข้อมูลและการประเมินยังคงสำคัญมาก
NLP และ Generative AI สำหรับเวชระเบียนและรายงานทางการแพทย์
งานด้านข้อความในสุขภาพครอบคลุมตั้งแต่การสกัดข้อมูลจากเวชระเบียนอิเล็กทรอนิกส์ (EHR), การสรุปเอกสารผู้ป่วย (clinical summarization), ไปจนถึงการช่วยเขียนรายงานทางการแพทย์และตอบคำถามทางคลินิก (clinical QA) โมเดล Transformer ขนาดใหญ่ เช่น BERT-based variants (BioBERT, ClinicalBERT), โมเดลทางการแพทย์เชิงสถาปัตยกรรมใหญ่เช่น GatorTron และโมเดล Generative เช่น Med-PaLM หรือการใช้ GPT-family ที่ได้รับการ fine-tune/controlled เป็นตัวอย่างที่นำมาใช้ในงานจริง
- การทำงาน: โมเดล Transformer ถูกใช้สำหรับ NER (การดึงชื่อโรค/ยา), relation extraction, และ abstractive summarization โดยประยุกต์การเรียนรู้จากข้อมูลคลินิกที่ได้รับการนิรนาม (de-identified) และเทคนิค RAG (retrieval-augmented generation) เพื่อเชื่อมคำตอบกับแหล่งความรู้ที่เชื่อถือได้
- กรณีใช้งานจริง: สรุป discharge summary อัตโนมัติ ลดเวลาการเขียนรายงานของแพทย์, สร้างร่างรายงานรังสีวิทยาที่แพทย์แก้ไขได้, ระบบช่วยตอบคำถามข้อมูลยา/ปริมาณการใช้ที่อิงกับแนวทางมาตรฐาน
Federated Learning และ Edge AI: ทางออกด้านความเป็นส่วนตัวและ latency
ความเป็นส่วนตัวของข้อมูลสุขภาพและความต้องการตอบสนองแบบเรียลไทม์ทำให้ Federated Learning และ Edge AI กลายเป็นเทคโนโลยีเชิงกลยุทธ์ Federated learning อนุญาตให้สถาบันหลายแห่งร่วมฝึกโมเดลโดยไม่ต้องรวมข้อมูลดิบไว้ที่ศูนย์กลาง โดยส่งพารามิเตอร์/gradients ที่ได้รับการนิรนาม (หรือผสมกับเทคนิค differential privacy) ตัวอย่างเฟรมเวิร์กที่ใช้ได้แก่ TensorFlow Federated, PySyft, Flower
- ข้อดี: ลดความเสี่ยงด้านข้อมูลผู้ป่วย, ช่วยให้โมเดลเรียนรู้จากข้อมูลที่หลากหลายทางประชากรศาสตร์, และลดข้อจำกัดทางกฎหมายเกี่ยวกับการเคลื่อนย้ายข้อมูล
- Edge AI: การรันโมเดลบนอุปกรณ์ใกล้จุดให้บริการ (เช่น เครื่องมือวินิจฉัยที่ bedside, เครื่องมือ imaging แบบพกพา) ช่วยลด latency และรักษาข้อมูลให้อยู่บนอุปกรณ์ ตัวอย่างเทคโนโลยีที่เกี่ยวข้องคือ ONNX, TensorRT, Core ML และฮาร์ดแวร์เช่น NVIDIA Jetson, Qualcomm AI Engine, Apple Neural Engine
- เทคนิครองรับ: model compression (pruning, quantization), knowledge distillation, และการออกแบบสถาปัตยกรรมขนาดเล็กเพื่อให้รันบน edge ได้จริง
โดยสรุป เทคโนโลยีเหล่านี้ร่วมกันสร้างระบบ AI ทางการแพทย์ที่มีความสามารถทั้งในการวิเคราะห์ภาพระดับสูง การสกัดและสรุปข้อมูลเชิงข้อความ และการให้บริการที่เป็นส่วนตัวและตอบสนองเร็ว การเลือกใช้เทคโนโลยีที่เหมาะสมต้องคำนึงถึงข้อกำหนดด้านความปลอดภัย ความเป็นส่วนตัว ความโปร่งใสของโมเดล และการบูรณาการเข้ากับเวิร์กโฟลว์ทางคลินิกเพื่อให้เกิดประโยชน์สูงสุดต่อผู้ป่วยและผู้ให้บริการดูแลสุขภาพ
กรณีศึกษาเชิงปฏิบัติ: ที่ไหนและอย่างไร AI ถูกใช้งานจริง
กรณีศึกษาเชิงปฏิบัติ: ที่ไหนและอย่างไร AI ถูกใช้งานจริง
ในเชิงปฏิบัติ ระบบปัญญาประดิษฐ์ (AI) ถูกนำไปใช้ในหลายจุดของการดูแลสุขภาพ ตั้งแต่การตรวจวินิจฉัยภาพถ่ายรังสี การวิเคราะห์ชิ้นเนื้อดิจิทัล การค้นคว้ายา การคัดกรองจีโนม การจัดลำดับความเร่งด่วนในบริการ telemedicine ไปจนถึงการติดตามผู้ป่วยด้วยอุปกรณ์สวมใส่ (wearable) ผลลัพธ์ที่วัดได้จากโครงการนำร่องและการศึกษาทางคลินิกจำนวนมากชี้ให้เห็นว่า AI สามารถเพิ่มความแม่นยำ ลดเวลา และเพิ่มประสิทธิภาพของระบบสุขภาพได้อย่างชัดเจน ข้อความต่อไปนี้สรุปตัวอย่างใช้งานที่จับต้องได้ ผลลัพธ์เชิงตัวเลข และอุปสรรคเชิงปฏิบัติที่พบในการนำไปใช้จริง
การอ่านภาพรังสี (X-ray/CT) — การประยุกต์ใช้ AI ในการช่วยอ่านภาพทรวงอกเพื่อค้นหามะเร็งปอดและปัญหาอื่น ๆ เป็นหนึ่งในกรณีที่มีหลักฐานรองรับมากที่สุด งานวิจัยหลายชิ้นรายงานว่าโมเดล AI ที่ผ่านการฝึกฝนร่วมกับ radiologist สามารถ เพิ่มอัตราการตรวจพบมะเร็งปอด เมื่อเทียบกับการอ่านด้วยสายตาเพียงอย่างเดียว โดยมีตัวเลขจากการศึกษาหลายงานระบุการเพิ่มขึ้นของความไว (sensitivity) ราว ๆ 10–20% ในสภาพแวดล้อมการตรวจคัดกรอง และช่วยลดอัตรา false negative ได้อย่างมีนัยสำคัญ นอกจากนี้ AI ยังช่วยลดเวลาการอ่านภาพของรังสีแพทย์ลงประมาณ 20–50% ในงานที่มีปริมาณภาพสูง ส่งผลให้ throughput ของแผนกรังสีดีขึ้นและเวลารอผลผู้ป่วยลดลง
การวิเคราะห์ชิ้นเนื้อดิจิทัล (Digital Pathology) — ระบบ deep learning สำหรับการวิเคราะห์สไลด์ทางพยาธิวิทยาสามารถจำแนกเนื้อร้าย ระบุขอบเขตเนื้องอก และให้คะแนนคุณภาพของชิ้นเนื้อได้อย่างรวดเร็ว งานวิจัยหลายโครงการสรุปว่า AI สามารถลดเวลาในการตรวจชิ้นเนื้อต่อเคสได้ตั้งแต่ 20–60% ในงานคัดกรอง และช่วยเพิ่มความสอดคล้องระหว่างผู้ตรวจ (inter-reader concordance) ซึ่งช่วยลดการต้องรีวิวซ้ำและส่งต่อผู้ป่วยอย่างมีประสิทธิภาพ
AlphaFold และผลกระทบต่อการค้นพบยาและชีววิทยาโครงสร้าง — ความก้าวหน้าของ AlphaFold ของ DeepMind แสดงให้เห็นถึงการเปลี่ยนแปลงเชิงพื้นฐานในการทำนายโครงสร้างโปรตีนโดยอาศัยข้อมูลลำดับกรดอะมิโน โดยฐานข้อมูลการคาดการณ์โครงสร้างที่เปิดเผยช่วยให้นักวิจัยสามารถเข้าถึงการคาดการณ์โครงสร้างโปรตีนจำนวนมหาศาลได้อย่างรวดเร็ว ผลลัพธ์เชิงปฏิบัติรวมถึงการเร่งกระบวนการค้นหาเป้าหมายยา (target identification) การออกแบบโมเลกุลที่ผูกกับโปรตีน และการลดความจำเป็นในการทดลองทางโครงสร้างที่ใช้เวลานาน ซึ่งในหลายกรณีช่วยย่นระยะเวลาขั้นต้นของการพัฒนายาได้หลายเดือนถึงหลายปี และช่วยลดต้นทุนการค้นคว้าต้นแบบ (lead discovery) อย่างมีนัยสำคัญ
การค้นพบและพัฒนายาโดยใช้ AI — บริษัทบιοเทคหลายรายใช้ AI เพื่อคัดกรองโมเลกุล คาดการณ์โพรไฟล์ความเป็นพิษ และออกแบบสารนำร่อง ผลที่วัดได้รวมถึงการลดระยะเวลาไปสู่การได้มาซึ่ง candidate ที่เหมาะสม (lead optimization) จากหลายปีเหลือเป็นเดือนถึงหนึ่งปีในบางโครงการ และการลดต้นทุนการค้นหาขั้นต้น ตัวอย่างเช่น บริษัทที่ใช้แพลตฟอร์ม generative chemistry และ predictive models รายงานการลดรอบเวลาการค้นเจอโมเลกุลนำร่องลงหลายสิบเปอร์เซ็นต์ และมีกรณีการเข้าสู่การทดลองทางคลินิกของยาออกแบบโดย AI เป็นครั้งแรกในช่วงไม่กี่ปีที่ผ่านมา
- การคัดกรองจีโนมและการวินิจฉัยทางพันธุกรรม — AI ถูกใช้วิเคราะห์ชุดข้อมูลจีโนมขนาดใหญ่เพื่อตรวจหาการกลายพันธุ์ที่สัมพันธ์กับโรค ผลลัพธ์เชิงตัวเลขจากโครงการนำร่องหลายแห่งชี้ว่า AI ช่วยเพิ่มอัตราการตรวจพบตัวแปรก่อโรค (pathogenic variants) ในผู้ป่วยที่สงสัยด้วยโรคพันธุกรรมได้ และช่วยลดเวลาวิเคราะห์ข้อมูลจากสัปดาห์เหลือวันหรือชั่วโมง ขณะเดียวกันระบบยังช่วยกรองผลลัพธ์ที่ไม่สำคัญออก ทำให้ผู้เชี่ยวชาญมุ่งจัดการกับกรณีที่มีนัยสำคัญ
- ระบบ triage ใน telemedicine — แพลตฟอร์ม telehealth ที่ผสานระบบ AI สำหรับ triage สามารถประเมินความเสี่ยงของผู้ป่วยเบื้องต้น แนะนำเส้นทางการรักษา และจัดลำดับความเร่งด่วนได้ โดยงานประเมินบางชุดพบว่า AI triage ช่วยลดเวลาการรอคอยเบื้องต้นลง 30–60% และเพิ่มความแม่นยำในการส่งต่อผู้ป่วยฉุกเฉิน ส่งผลให้ทรัพยากรทางการแพทย์ถูกจัดสรรได้อย่างคุ้มค่าขึ้น
- การใช้ wearable เพื่อติดตามผู้ป่วย — อุปกรณ์สวมใส่ที่ติดตั้งโมเดล AI สามารถตรวจจับภาวะผิดปกติ เช่น ภาวะหัวใจเต้นผิดจังหวะ (atrial fibrillation) หรือการเปลี่ยนแปลงของสัญญาณชีวนิรภัยได้แบบต่อเนื่อง การศึกษาหลายชิ้นแสดงว่า wearable-enabled detection มี predictive value สูง (เช่น PPV >80% ในบางการศึกษาสำหรับการแจ้งเตือน AFib) และเมื่อนำมาผสานกับการติดตามเชิงรุกสามารถลดการเข้าโรงพยาบาลฉุกเฉินได้บางส่วน
- GenAI ในการสรุป EMR (Electronic Medical Records) — ระบบภาษาธรรมชาติแบบใหญ่ (GenAI) ถูกใช้งานเพื่อสรุปบันทึกการรักษา สร้างสรุปเคส และร่างบันทึกทางคลินิกอัตโนมัติ รายงานจากการนำร่องในโรงพยาบาลบางแห่งระบุว่าเทคโนโลยีนี้ช่วยลดเวลาการกรอกเอกสารของแพทย์ได้ หลายชั่วโมงต่อสัปดาห์ (โดยทั่วไปประมาณ 2–8 ชั่วโมงต่อสัปดาห์ ขึ้นอยู่กับภาระงานและระดับการปรับใช้งาน) ทำให้แพทย์มีเวลามากขึ้นในการดูแลผู้ป่วยตรงหน้าและลดภาระงานที่ไม่ใช่การรักษา
อุปสรรคที่พบในการนำไปใช้จริง — แม้ผลลัพธ์จะเป็นที่น่าพอใจ แต่การบูรณาการ AI ในบริบทการดูแลสุขภาพยังเผชิญอุปสรรคหลายประการ ได้แก่
- ข้อมูลและความเอนเอียง (data bias): โมเดลที่ฝึกบนข้อมูลไม่หลากหลายอาจทำงานได้ไม่ดีในประชากรอื่น ทำให้เกิดความไม่เสมอภาคในการวินิจฉัย
- การอนุญาตและการรับรองทางกฎหมาย (regulatory): ผลิตภัณฑ์ AI ทางการแพทย์ต้องผ่านการรับรองจากหน่วยงานกำกับดูแล (เช่น FDA/CE) ซึ่งต้องมีการศึกษาทางคลินิกและหลักฐานด้านความปลอดภัย/ประสิทธิผล
- การรวมกับเวิร์กโฟลว์ของคลินิกและ EHR: การเชื่อมต่อที่ไม่ดีจะทำให้ผู้ใช้งานเกิดภาระงานเพิ่มและขัดขวางการนำไปใช้งานจริง
- ความโปร่งใสและการอธิบายเหตุผลได้ (explainability): แพทย์มักต้องการคำอธิบายว่าระบบตัดสินใจอย่างไร เพื่อใช้ประกอบการตัดสินใจทางการแพทย์
- ความเป็นส่วนตัวและความปลอดภัยของข้อมูล: การจัดการจีโนมและข้อมูลสุขภาพที่มีความละเอียดอ่อนต้องมีมาตรการคุ้มครองข้อมูลที่เข้มงวด
- โมเดลการชำระเงินและค่าตอบแทน: ในหลายภูมิภาคยังไม่มีกรอบการชำระเงินที่ชัดเจนสำหรับบริการที่ใช้ AI ซึ่งเป็นอุปสรรคต่อการลงทุนและการปรับใช้ในวงกว้าง
สรุปคือ เทคโนโลยี AI ในวงการสุขภาพได้แสดงผลลัพธ์เชิงปฏิบัติที่จับต้องได้ทั้งในด้านความแม่นยำและประสิทธิภาพการดำเนินงาน แต่การนำไปสู่การใช้งานเชิงพาณิชย์ระยะยาวจำเป็นต้องมีการยืนยันความคงที่ของผลลัพธ์ในประชากรหลากหลาย ปรับปรุงการเชื่อมต่อกับระบบคลินิก ตลอดจนกรอบการกำกับดูแลและโมเดลค่าตอบแทนที่เหมาะสม เพื่อให้โรงพยาบาลและผู้ให้บริการสามารถเก็บเกี่ยวประโยชน์จาก AI ได้อย่างปลอดภัยและยั่งยืน
ผลกระทบต่อการดำเนินงาน งานบุคลากร และการเงินของระบบสุขภาพ
ผลกระทบต่อการดำเนินงาน งานบุคลากร และการเงินของระบบสุขภาพ
การนำระบบปัญญาประดิษฐ์ (AI) เข้ามาใช้ในระบบสุขภาพมีผลกระทบเชิงปฏิบัติอย่างเป็นรูปธรรมต่อกระบวนการทำงาน (workflow) โครงสร้างงาน และงบประมาณของหน่วยบริการสุขภาพ ในด้านการดำเนินงาน ตัวอย่างที่ชัดเจนคือหน่วยรังสีซึ่งงานวิจัยและการนำไปปฏิบัติจริงรายงานว่าการใช้โมเดลช่วยอ่านภาพสามารถลดเวลาในการอ่านผลต่อเคสได้ในช่วง ประมาณ 20–50% ขึ้นอยู่กับประเภทภาพและระดับการผนวกรวมของระบบผลคือการเพิ่ม throughput ของงานรังสีได้ระหว่าง 30–70% ในกรณีที่มีการจัด workflow ให้ AI ทำการคัดกรองและจัดลำดับความสำคัญกรณีฉุกเฉิน (triage) ก่อนหมอจะอ่านจริง ซึ่งส่งผลโดยตรงต่อลดเวลารอผลการอ่านและลดเวลา-to-treatment สำหรับผู้ป่วยเฉียบพลันได้ชัดเจน
ในแง่งานบุคลากร จะเกิดการเปลี่ยนบทบาทชัดเจนจากงานปฏิบัติ (hands-on interpretation/annotation) ไปเป็นงานตรวจสอบ ปรับแต่ง และควบคุมคุณภาพของ AI (AI oversight and model stewardship) แพทย์รังสีและพยาธิแพทย์บางส่วนจะทำหน้าที่เป็นผู้ตรวจสอบผลที่ AI สร้าง พร้อมทั้งรับผิดชอบการตัดสินใจสุดท้ายและการจัดการเคสที่มีความไม่แน่นอน มากกว่าจะเป็นผู้ทำการวิเคราะห์ภาพจากศูนย์เริ่มต้น ตัวเลขประมาณการจากหน่วยบริการที่เริ่มใช้ AI ชี้ว่าในระยะเริ่มต้นอาจต้องใช้เวลาในการฝึกอบรมเพิ่มขึ้น 40–120 ชั่วโมง/คน สำหรับการใช้งานระบบใหม่ การประยุกต์วิชาชีพและการโยกย้ายงานนี้อาจทำให้ตำแหน่งบางประเภทลดลงในเชิงปริมาณ แต่ทำให้เกิดตำแหน่งใหม่ เช่น ผู้ดูแลโมเดล (model curator), วิศวกรข้อมูลทางการแพทย์ และผู้ประสานงานด้าน AI กับการดูแลคลินิก
ด้านการเงิน แม้ค่าใช้จ่ายเริ่มต้น (capital expenditure และค่า integration) จะสูง—รวมถึงค่าซอฟต์แวร์ การเชื่อมต่อกับ PACS/EHR ค่า license รายปี และต้นทุนคลาวด์สำหรับการประมวลผลภาพ—การวิเคราะห์ทางเศรษฐศาสตร์หลายฉบับชี้ว่า AI มีศักยภาพในการลดต้นทุนการดูแลในระยะยาวได้สำคัญ ตัวอย่างการประมาณการเชิงอนุกรมพบว่า: ระยะคืนทุน (payback period) สำหรับโครงการ AI ในหน่วยรังสีมักอยู่ในช่วง 12–36 เดือน หากมีอัตราการใช้งานสูงและปรับ workflow ได้เต็มที่ และการประหยัดต้นทุนปฏิบัติการ (operational savings) อาจมีค่าเฉลี่ย 10–25% ของต้นทุนการดำเนินงานต่อปีในช่วง 3–5 ปีแรกเมื่อรวมการลดเวลาทำงาน การลดการสแกนซ้ำและการลด length of stay ที่สัมพันธ์กับการวินิจฉัยเร็วขึ้น
- ตัวชี้วัดคุณภาพและผลลัพธ์ (outcomes): ควรวัดทั้งความแม่นยำ (sensitivity/specificity), เวลาในการออกผล (turnaround time), เวลา-to-treatment, อัตราการส่งกลับ (readmission) และ length of stay — ตัวอย่างคือการวินิจฉัยเร็วขึ้น 20–40% อาจสัมพันธ์กับการลด LOS ประมาณ 5–15% ในบางผู้ป่วยเฉพาะโรค
- ROI และการประเมินต้นทุน: ควรรวมค่าใช้จ่ายแฝง เช่น ค่า label ข้อมูล (data annotation), การดูแลรักษาโมเดล (monitoring/validation), ค่าประกันความเสี่ยง และค่า training ต่อบุคลากร การคำนวณ ROI ที่เป็นธรรมควรรวมประโยชน์ทั้งทางการเงิน (ลดค่าใช้จ่ายโดยตรง) และประโยชน์เชิงคุณภาพ (ลดความผิดพลาดทางการแพทย์ และเพิ่มความพึงพอใจของผู้ป่วย)
- การเปลี่ยนแปลง workflow ที่แนะนำ: ผนวกรวม AI เข้ากับ PACS/EHR (ไม่ใช่ระบบแยกเดี่ยว), ตั้งกลไกการตรวจสอบผลโดยผู้เชี่ยวชาญ, ใช้ AI เป็นเครื่องมือคัดกรอง (triage) และใช้ automation ในการกรอกข้อมูลเบื้องต้นของรายงานเพื่อลดเวลาการพิมพ์และการทำซ้ำ
- ความเสี่ยงและต้นทุนระยะยาว: ภาระการกำกับดูแลและความรับผิดชอบทางกฎหมายอาจเพิ่มขึ้น หากไม่มีการประเมินและตรวจสอบอย่างต่อเนื่อง นอกจากนี้ค่าใช้จ่ายด้านการอัปเดตและการตรวจสอบโมเดลอาจเป็นต้นทุนที่ต้องเผื่อไว้ในงบประมาณประจำปี
สรุปคือการนำ AI เข้าสู่ภาคการดูแลสุขภาพมีศักยภาพในการปรับปรุงประสิทธิภาพการดำเนินงาน เพิ่ม throughput โดยเฉพาะในหน่วยรังสี และลดต้นทุนระยะยาว แต่ต้องแลกด้วยค่าใช้จ่ายเริ่มต้นและการลงทุนในการฝึกอบรมบุคลากร การออกแบบ workflow ใหม่ และการบริหารความเสี่ยงเชิงกฎหมายและคุณภาพ องค์กรที่วางแผนการนำ AI มาใช้ควรประเมินผลประโยชน์และต้นทุนอย่างเป็นระบบ โดยตั้ง KPI ที่ชัดเจนทั้งด้านเวลา คุณภาพ และค่าใช้จ่ายเพื่อติดตาม ROI ในทุกช่วงของการดำเนินโครงการ
ความท้าทายเชิงข้อมูล จริยธรรม และกฎระเบียบ
Bias ในข้อมูลและผลกระทบต่อความเป็นธรรม
หนึ่งในความเสี่ยงที่สำคัญที่สุดของการนำ AI มาใช้ในระบบสุขภาพคือ ข้อมูลที่ไม่สมดุล (data imbalance) ซึ่งนำไปสู่ผลลัพธ์ที่ไม่เป็นธรรมต่อกลุ่มประชากรย่อย เช่น เพศ เชื้อชาติ อายุ หรือพื้นที่ทางภูมิศาสตร์ งานวิจัยและการศึกษาในช่วงหลายปีที่ผ่านมาแสดงให้เห็นว่าโมเดลการวินิจฉัยและการคัดกรองบางชนิดมักมีประสิทธิภาพลดลงอย่างมีนัยสำคัญสำหรับกลุ่มตัวอย่างที่มีตัวแทนน้อย ข้อมูลไม่ครอบคลุมสามารถทำให้เกิดการวินิจฉัยพลาดหรือการให้บริการรักษาที่ไม่เหมาะสม ซึ่งอาจส่งผลด้านสุขภาพและความเชื่อมั่นของผู้ป่วยได้
ตัวอย่างเชิงปฏิบัติที่พบได้บ่อยคือชุดข้อมูลจากโรงพยาบาลขนาดใหญ่ในเมืองอาจมีประชากรที่แตกต่างจากชุมชนชนบท ทำให้โมเดลที่ฝึกจากข้อมูลเหล่านั้นไม่สามารถทั่วไปได้ ผลกระทบบางกรณีอาจลดความแม่นยำลงได้เป็น หลายสิบเปอร์เซ็นต์ ในกลุ่มที่ไม่ได้รับการแทนค่าอย่างเหมาะสม ซึ่งในเชิงธุรกิจหมายถึงความเสี่ยงต่อความน่าเชื่อถือของผลิตภัณฑ์และความรับผิดทางกฎหมาย

ความโปร่งใส (Explainability) และการตรวจสอบแบบต่อเนื่อง
การอธิบายผลลัพธ์ของโมเดล (explainability) ไม่ใช่เพียงข้อกำชับทางจริยธรรมแต่เป็นข้อกำหนดเชิงปฏิบัติในการใช้งานทางคลินิก ผู้ให้บริการด้านสุขภาพต้องการทราบเหตุผลเบื้องหลังคำแนะนำจาก AI เพื่อประกอบการตัดสินใจร่วมกับผู้ป่วย นอกจากนั้นยังจำเป็นต้องมีการตรวจสอบแบบต่อเนื่อง (continuous monitoring) เพื่อจับการเปลี่ยนแปลงของข้อมูล (data drift) และประสิทธิภาพของโมเดลในสภาพแวดล้อมจริง
การตรวจสอบต้องรวมถึงการรายงานประสิทธิภาพตามกลุ่มย่อย (stratified performance metrics), การตั้งเกณฑ์เตือนเมื่อประสิทธิภาพตกต่ำ (alerting thresholds), การเก็บและวิเคราะห์ log เพื่อหาเหตุแห่งความผิดพลาด และการทดสอบย้อนกลับ (backtesting) เป็นระยะๆ เพื่อให้แน่ใจว่าโมเดลยังคงปลอดภัยและยุติธรรมต่อผู้ป่วยทุกกลุ่ม
ความรับผิดชอบทางกฎหมาย และกรอบกฎระเบียบที่กำลังพัฒนา
กรอบกฎระเบียบที่เกี่ยวข้องกับ AI ในสุขภาพกำลังพัฒนาอย่างรวดเร็ว ทั้งระดับสากลและระดับประเทศ ตัวอย่างที่สำคัญได้แก่ FDA AI/ML Action Plan ซึ่งเน้นการกำกับดูแลซอฟต์แวร์ทางการแพทย์ที่ใช้การเรียนรู้ของเครื่องด้วยการให้ความสำคัญกับการตรวจสอบวงจรชีวิตของโมเดลและการอัปเดตในภายหลัง ส่วนในสหภาพยุโรป EU AI Act ตั้งระดับความเสี่ยงตามประเภทแอปพลิเคชันและกำหนดข้อบังคับเข้มงวดสำหรับระบบที่มีความเสี่ยงสูง (high-risk AI)
สำหรับประเทศไทย กฎหมายคุ้มครองข้อมูลส่วนบุคคล (PDPA) ที่บังคับใช้ในเชิงปฏิบัติได้ตั้งแต่ปี 2565 เป็นพื้นฐานสำคัญ ขณะเดียวกันหน่วยงานภาครัฐและสถาบันวิชาการกำลังพัฒนาแนวทางด้านจริยธรรมและมาตรฐานการทดสอบสำหรับ AI ทางการแพทย์ ซึ่งองค์กรธุรกิจควรติดตามการประกาศเชิงนโยบายและการตีความข้อกฎหมายอย่างใกล้ชิดเพื่อลดความเสี่ยงทางกฎหมายและการกำกับดูแล
แนวทางปฏิบัติที่แนะนำ: Governance, Validation Protocols และ Audit Trails
เพื่อลดความเสี่ยงทางข้อมูล จริยธรรม และกฎระเบียบ องค์กรควรนำแนวทางการบริหารจัดการ AI ที่เข้มแข็งมาปฏิบัติจริง โดยข้อเสนอแนะสำคัญได้แก่
- จัดตั้งโครงสร้างการกำกับดูแล (AI governance) เช่น คณะกรรมการ AI ข้ามหน่วยงานที่รวมฝ่ายคลินิก ฝ่ายกฎหมาย ฝ่ายเทคนิค และฝ่ายบริหารความเสี่ยง เพื่อกำหนดนโยบายการใช้ข้อมูล มาตรฐานความยุติธรรม และการอนุมัติการนำระบบสู่การใช้งานจริง
- ออกแบบมาตรฐานการตรวจรับ (validation protocols) ที่รวมทั้งการทดสอบเชิงเทคนิคและการทดสอบทางคลินิก ก่อนนำโมเดลขึ้นสู่ระบบจริง รวมถึงการทดสอบตามกลุ่มย่อย (subgroup analysis) และการทดสอบความทนต่อการเปลี่ยนแปลงของข้อมูล
- สร้าง audit trails และการบันทึกข้อมูลที่ครบถ้วน เพื่อให้สามารถย้อนกลับตรวจสอบการตัดสินใจของระบบได้ (provenance, versioning, access logs) ซึ่งเป็นหลักฐานสำคัญเมื่อเกิดข้อโต้แย้งหรือการตรวจสอบจากหน่วยงานกำกับดูแล
- นำแนวปฏิบัติด้านความเป็นส่วนตัวและความปลอดภัยมาใช้อย่างเคร่งครัด เช่น differential privacy, federated learning สำหรับการฝึกและใช้งานโมเดลข้ามสถาบัน และการเข้ารหัสข้อมูล (encryption) ทั้งขณะเก็บและระหว่างการส่ง
- ติดตั้งระบบตรวจจับ drift และกลไกการรีเทรนตามกำหนด พร้อมเกณฑ์เชิงปริมาณสำหรับการเรียกกลับ (rollback) หรือการระงับการใช้งานเมื่อพบความเสี่ยง
- จัดให้มีการตรวจสอบอิสระ (third-party audits) และการเผยแพร่เอกสารกำกับ เช่น model cards และ datasheets เพื่อเพิ่มความโปร่งใสต่อผู้ใช้และผู้กำกับดูแล
สรุปได้ว่า การนำ AI เข้าสู่ระบบสุขภาพอย่างยั่งยืนจำเป็นต้องมีการจัดการข้อมูลที่รัดกุม การออกแบบระบบที่โปร่งใสและสามารถอธิบายผลได้ และกรอบการกำกับดูแลที่ชัดเจน ทั้งนี้องค์กรที่ลงทุนในนโยบายด้าน governance, การตรวจสอบ และเอกสารประกอบที่เหมาะสมจะสามารถลดความเสี่ยง ทั้งด้านจริยธรรมและกฎหมาย พร้อมสร้างความเชื่อมั่นให้กับผู้ป่วยและผู้ร่วมงานในระยะยาว
การลงทุน ตลาด และนโยบายสาธารณะที่ควรติดตาม
การลงทุนและแนวโน้มตลาด
การลงทุนในสตาร์ทอัพด้าน AI เพื่อสุขภาพยังคงเติบโตอย่างต่อเนื่อง แม้จะมีสภาวะตลาดที่ผันผวนในช่วงปี 2021–2023 รายงานจากสถาบันวิจัยหลายแห่งระบุว่าเม็ดเงินจาก VC และการลงทุนเชิงกลยุทธ์ของบริษัทยักษ์ใหญ่ (corporate investment) เพิ่มขึ้นหลายเท่าตัวเมื่อเทียบกับช่วงก่อนหน้า โดยมีการระดมทุนทั้งในรูปแบบ Seed/Series และการเข้าซื้อกิจการเชิงเทคโนโลยีที่มีมูลค่าระดับสูง ตัวเลขจากการสำรวจทั่วโลกชี้ว่าอุตสาหกรรม AI ในสุขภาพอาจมีมูลค่าตลาดเป็นระดับหลายหมื่นล้านดอลลาร์ภายในต้นทศวรรษ 2030s โดยประมาณอัตราการเติบโตต่อปี (CAGR) อยู่ในกรอบกว้างตามรายงานต่างประเทศ
อย่างไรก็ตาม นักลงทุนในรอบหลังให้ความสำคัญกับการพิสูจน์คุณค่าทางคลินิกและเศรษฐศาสตร์ มากกว่าการเติบโตของผู้ใช้เพียงอย่างเดียว due diligence ด้านผลลัพธ์ทางคลินิก (clinical outcomes), การยอมรับจากระบบสุขภาพ, และเส้นทางการชำระเงินคืนกลายเป็นตัวกรองหลัก ส่งผลให้รอบการระดมทุนอาจยืดออกและมุ่งไปยังสตาร์ทอัพที่สามารถแสดงหลักฐานและโมเดลธุรกิจที่ชัดเจนได้
การชำระเงินคืน (Reimbursement) และโมเดลธุรกิจที่ต้องจับตามอง
หนึ่งในปัจจัยกำหนดความสำเร็จเชิงพาณิชย์ของ AI ทางการแพทย์คือความชัดเจนของการชำระเงินคืน — เช่นการมีรหัสค่าบริการที่ชัดเจน (ในสหรัฐฯ อ้างอิงเช่น CPT codes) หรือแนวทางการจ่ายเงินจากหน่วยงานชำระเงินของแต่ละประเทศ ในหลายประเทศ ผู้จ่ายเงินเริ่มพิจารณาการจ่ายเงินสำหรับซอฟต์แวร์การวินิจฉัยหรือการช่วยตัดสินใจ (SaMD) ผ่านโครงการชั่วคราวหรือการประเมินความคุ้มค่า
ดังนั้น โมเดลธุรกิจที่น่าสนใจในอีกข้างหน้าจะเป็นรูปแบบที่มีรายการชำระเงินชัดเจนหรือสามารถชี้วัดผลลัพธ์เพื่อรองรับสัญญาการชำระเงินตามผลลัพธ์ (outcomes‑based contracts) เช่น การคิดค่าบริการแบบ subscription บวกค่าตามผลลัพธ์ที่วัดได้ (reduced LOS, ลดการกลับมารักษา, ประหยัดต้นทุนต่อผู้ป่วย) หรือการขายสิทธิใช้งานร่วมกับการแบ่งผลประหยัดกับผู้ให้บริการสุขภาพ (risk-sharing) นอกจากนี้ การออกแบบเพื่อให้สอดคล้องกับมาตรฐานการเรียกเก็บค่าบริการของระบบสาธารณสุขจะช่วยลดอุปสรรคทางการเงินสำหรับการนำไปใช้จริง
นโยบายสาธารณะและปัจจัยเร่งการนำ AI มาใช้
ภาครัฐและหน่วยงานกำกับดูแลมีบทบาทสำคัญในการเร่งหรือชะลอการนำ AI มาใช้ในระบบสุขภาพ โดยนโยบายที่กระตุ้นการใช้ได้แก่ การจัดสรรงบประมาณสนับสนุนการทดลองและการวิจัยเชิงประยุกต์, การออกแนวทางด้านการกำกับดูแลที่ชัดเจน (regulatory pathways) สำหรับซอฟต์แวร์ทางการแพทย์, การกำหนดกรอบการคุ้มครองข้อมูลผู้ป่วยที่เอื้อต่อการใช้ข้อมูลเพื่อการพัฒนา AI และมาตรการจูงใจด้านการจัดซื้อสาธารณะ (procurement incentives) สำหรับเทคโนโลยีที่พิสูจน์ผลดี
ตัวอย่างเชิงนโยบายที่ควรติดตามได้แก่การปรับปรุงกฎเกณฑ์ของหน่วยงานกำกับยาและอุปกรณ์การแพทย์ในภูมิภาคต่าง ๆ, โครงการประเมินเทคโนโลยีสุขภาพระดับชาติ (HTA) ที่เพิ่มการพิจารณา AI, และนโยบายการชำระเงินคืนที่เริ่มครอบคลุมซอฟต์แวร์แพทย์ หากมีการกำหนดมาตรฐานการวัดผลลัพธ์ร่วมกัน จะช่วยให้ผู้พัฒนาและผู้ชำระเงินสื่อสารกันได้ชัดเจนขึ้นและลดความเสี่ยงจากการลงทุน
คำแนะนำเชิงกลยุทธ์สำหรับสตาร์ทอัพและโรงพยาบาล
- สตาร์ทอัพ: ลงทุนในหลักฐานเชิงคลินิก (RCTs, pragmatic trials, real‑world evidence) ตั้งแต่ระยะต้น วางแผนเส้นทางการขึ้นทะเบียนและการขอรหัสค่าบริการควบคู่ไปกับการพัฒนาผลิตภัณฑ์ โดยกำหนดตัวชี้วัดที่ชัดเจน (เช่น ลดระยะเวลาอยู่โรงพยาบาล, ลดการอ่านซ้ำ) เพื่อใช้เป็นข้อพิสูจน์ค่าใช้จ่ายและประโยชน์ต่อผู้จ่ายเงิน
- ความร่วมมือกับระบบสุขภาพ: ตั้งพันธมิตรเชิงกลยุทธ์กับโรงพยาบาลขนาดใหญ่เพื่อทำงานร่วมกันในโปรแกรมนำร่อง (pilot) และเก็บข้อมูลเชิงปฏิบัติการ การทำงานแบบ co‑development ช่วยให้การติดตั้งและการยอมรับภายในคลินิกรวดเร็วขึ้น
- โมเดลการชำระเงิน: ออกแบบโมเดลการชำระเงินที่ยืดหยุ่น เช่น subscription + performance incentives หรือสัญญาแบ่งผลประหยัด (shared‑savings) เพื่อเอื้อต่อการทดลองใช้ในระบบที่มีงบประมาณจำกัด และเตรียมเอกสารเพื่อขอรหัสค่าบริการ/การขึ้นบัญชีจากผู้จ่ายเงิน
- โรงพยาบาลและผู้ให้บริการ: จัดตั้งหน่วยประเมินเทคโนโลยี AI ภายใน ร่วมกับทีมคลินิก ไอที และการเงิน เพื่อประเมินความคุ้มค่าและความเสี่ยง สร้างโครงสร้างพื้นฐานข้อมูลและมาตรการคุ้มครองข้อมูล (governance) ที่เอื้อต่อการทดสอบและนำระบบ AI เข้าสู่การปฏิบัติ
- การปฏิบัติและการวัดผล: ทั้งสองฝ่ายควรตกลงชุดตัวชี้วัดก่อนการทดลอง เพื่อลดความเสี่ยงด้านการประเมินผลและรองรับข้อเรียกร้องการชำระเงินคืน การวัดผลที่ชัดเจนจะช่วยเพิ่มความน่าเชื่อถือต่อผู้ลงทุนและหน่วยงานกำกับ
สรุปคือ ภายในทศวรรษหน้า โอกาสการเติบโตของ AI ในวงการสุขภาพยังสูง แต่ความสำเร็จเชิงพาณิชย์จะขึ้นกับการสร้างหลักฐานที่ชัดเจน, การวางแผนเส้นทางการชำระเงินคืนตั้งแต่ระยะแรก, และการสร้างความร่วมมือเชิงกลยุทธ์ระหว่างสตาร์ทอัพ โรงพยาบาล และผู้จ่ายเงิน การติดตามนโยบายสาธารณะและการปรับตัวให้สอดคล้องจะเป็นปัจจัยสำคัญที่แยกผู้ชนะออกจากผู้ที่ล้มเหลวในตลาดนี้
มุมมองถึงปี 2034: สถานการณ์ที่น่าจับตามองและคำแนะนำเชิงปฏิบัติ
ในรอบทศวรรษข้างหน้า (2024–2034) การประยุกต์ใช้ปัญญาประดิษฐ์ในระบบสุขภาพมีแนวโน้มที่จะเปลี่ยนโฉมการดูแลผู้ป่วยอย่างเป็นรูปธรรม ทั้งในระดับการวินิจฉัย การรักษา และการบริหารจัดการทรัพยากร บทสรุปต่อไปนี้นำเสนอ 4 สถานการณ์ที่เป็นไปได้ซึ่งผู้บริหารโรงพยาบาล ผู้พัฒนาเทคโนโลยี และผู้กำหนดนโยบายควรจับตามอง พร้อมคำแนะนำเชิงปฏิบัติที่ใช้ได้จริง
สถานการณ์ที่ 1: GenAI และโมเดลทางการแพทย์เป็นกระแสหลักในงานคลินิก
ภายในปี 2034 การใช้งาน Generative AI (เช่น การสรุปประวัติผู้ป่วย การช่วยเขียนรายงาน และการสนับสนุนการตัดสินใจทางคลินิก) จะกลายเป็นส่วนหนึ่งของกระบวนการคลินิกปกติ การบูรณาการกับระบบบันทึกสุขภาพอิเล็กทรอนิกส์ (EHR) จะลึกขึ้น ทำให้ข้อมูลเชิงบริบทถูกนำไปใช้แบบเรียลไทม์ ตัวอย่างเช่น งานวิจัยและโครงการนำร่องหลายแห่งรายงานว่าการใช้โมเดลช่วยอ่านภาพรังสีและสรุปรายงานสามารถลดเวลาการอ่านและรอผลได้ 20–40% ในเคสที่เหมาะสม
สถานการณ์ที่ 2: กฎระเบียบและมาตรฐานเพื่อความปลอดภัยและความเป็นธรรมเข้มงวดขึ้น
รัฐบาลและหน่วยงานกำกับดูแลทั่วโลกจะเพิ่มมาตรฐานเพื่อคุ้มครองผู้ป่วยจากความเสี่ยงด้านความปลอดภัย ความเป็นส่วนตัว และอคติของโมเดล (algorithmic bias) คาดว่าจะมีการออกประกาศมาตรฐานการทดสอบเชิงคลินิกสำหรับ AI ระบบการตรวจสอบคุณภาพข้อมูล และกรอบการประเมินความเสี่ยงก่อนอนุญาตใช้งานในคลินิก การไม่ปฏิบัติตามมาตรฐานเหล่านี้อาจทำให้การนำไปใช้ถูกระงับหรือมีค่าใช้จ่ายด้านการปฏิบัติตามสูงขึ้น
สถานการณ์ที่ 3: AI เป็นพื้นฐานของการแพทย์เฉพาะบุคคล (Precision Medicine)
ด้วยการรวมข้อมูลจีโนมิก ข้อมูลไลฟ์สไตล์ และสัญญาณชีวภาพจากอุปกรณ์สวมใส่ AI จะช่วยปรับแผนการรักษาให้เหมาะสมกับผู้ป่วยแต่ละรายได้มากขึ้น ทั้งนี้ การลงทุนในชุดข้อมูลที่มีคุณภาพสูงและการสร้างมาตรฐานการแลกเปลี่ยนข้อมูลจะเป็นปัจจัยสำคัญ ตัวอย่างเช่น การวิเคราะห์หลายตัวบ่งชี้ร่วมกันโดย AI อาจช่วยคาดการณ์การตอบสนองต่อยาได้แม่นยำขึ้น ทำให้ลดการทดลองผิดพลาดและเพิ่มประสิทธิผลการรักษา
สถานการณ์ที่ 4: การเปลี่ยนแปลงแรงงานและระบบทักษะ (Workforce Transformation)
การนำ AI มาใช้ในวงการสุขภาพจะเปลี่ยนบทบาทของบุคลากรทางการแพทย์จากงานเชิงปฏิบัติการซ้ำซ้อน ไปสู่การวิเคราะห์เชิงวิพากษ์และการดูแลเชิงมนุษยสัมพันธ์ ส่งผลให้มีความต้องการทักษะด้านข้อมูล (data literacy), การตีความผลลัพธ์จากโมเดล และทักษะการจัดการการเปลี่ยนแปลง คาดว่าองค์กรที่ไม่ลงทุนในการฝึกอบรมซ้ำ (retraining/upskilling) อาจเผชิญช่วงการขาดแคลนบุคลากรที่ปรับตัวได้
สถิติสำคัญ: งานสำรวจเชิงสากลในช่วง 2022–2024 ชี้ว่า 40–70% ขององค์กรดูแลสุขภาพมีโครงการ AI อย่างน้อยหนึ่งโครงการ และโครงการที่บูรณาการกับ EHR มีแนวโน้มเพิ่มขึ้นทุกปี
คำแนะนำเชิงปฏิบัติ: Roadmap และเช็คลิสต์สำหรับผู้บริหาร โรงพยาบาล ผู้พัฒนา และผู้กำหนดนโยบาย
-
สำหรับผู้บริหารโรงพยาบาล — Roadmap 3 ระยะ
- ระยะสั้น (1–2 ปี): ประเมินสภาพข้อมูลในองค์กร (data maturity assessment), ตั้งคณะกรรมการ AI governance, เริ่มโครงการนำร่อง (pilot) ที่มีขอบเขตชัดเจน และวัดผลที่สำคัญ (KPI) เช่น ความแม่นยำ เวลาในการตัดสินใจ ความพึงพอใจของผู้ป่วย
- ระยะกลาง (3–5 ปี): ขยายการบูรณาการ AI กับ EHR ในโมดูลที่ปลอดภัย ตั้งกระบวนการตรวจสอบ (continuous monitoring) ของผลลัพธ์และอคติ จัดโปรแกรมฝึกอบรมบุคลากรด้าน data literacy และ clinical AI workflows
- ระยะยาว (6–10 ปี): บูรณาการ AI เป็นส่วนหนึ่งของ care pathways, ลงทุนในสถาปัตยกรรมข้อมูลแบบเปิด (interoperable data architecture), และร่วมมือกับหน่วยงานวิจัยเพื่อพัฒนาการรักษาแบบจำเพาะบุคคล
-
สำหรับผู้พัฒนาและผู้จัดจำหน่ายเทคโนโลยี — เช็คลิสต์การพัฒนาและปรับใช้
- ออกแบบระบบโดยคำนึงถึงความโปร่งใส (explainability) และการตรวจสอบ (audit trails)
- ทดสอบความเป็นธรรม (bias testing) และประสิทธิภาพบนชุดข้อมูลที่หลากหลายทางประชากรศาสตร์
- ให้ความสำคัญกับการปกป้องข้อมูลผู้ป่วย (data privacy) และใช้มาตรการ security-by-design
- พัฒนาชุดเอกสารที่ชัดเจนสำหรับผู้ใช้ทางคลินิก รวมทั้งการฝึกอบรมและคู่มือการใช้งาน
- วางแผนการสนับสนุนหลังการติดตั้ง (post-deployment support) และเครื่องมือสำหรับการตรวจสอบประสิทธิภาพอย่างต่อเนื่อง
-
สำหรับผู้กำหนดนโยบาย — แนวทางนโยบายและมาตรการ
- กำหนดกรอบการอนุมัติที่ชัดเจนสำหรับ AI ทางการแพทย์ รวมถึงเกณฑ์การทดสอบความปลอดภัยและความเป็นธรรม
- ส่งเสริมมาตรฐานการแลกเปลี่ยนข้อมูล (interoperability standards) เพื่อหลีกเลี่ยงการล็อกข้อมูล (data lock-in)
- จัดตั้งกลไกการตรวจสอบความเสี่ยงและการรายงานเหตุไม่พึงประสงค์จากระบบ AI
- สนับสนุนโครงการฝึกอบรมแรงงานด้านสุขภาพและการวิจัยเชิงประยุกต์ที่รวม AI
- พิจารณานโยบายด้านความรับผิดชอบทางกฎหมาย (liability frameworks) ที่สมดุลระหว่างนวัตกรรมและการปกป้องผู้ป่วย
โดยสรุป การเตรียมตัวตั้งแต่วันนี้ — ทั้งการลงทุนในข้อมูลที่มีคุณภาพ สร้างโครงสร้างกำกับดูแลภายในที่แข็งแรง และการเตรียม workforce retraining — จะเป็นปัจจัยกำหนดความสำเร็จของการนำ AI เข้าสู่วงการสุขภาพในอีกหนึ่งทศวรรษข้างหน้า องค์กรที่มีแผนงานชัดเจนและยืดหยุ่นต่อการเปลี่ยนแปลงจะสามารถเก็บเกี่ยวประโยชน์ทางคลินิกและเชิงเศรษฐกิจจาก AI ได้อย่างยั่งยืน
บทสรุป
AI มีศักยภาพเปลี่ยนแปลงระบบสุขภาพอย่างลึกซึ้ง ทั้งในด้านการวินิจฉัย การติดตามผู้ป่วย การจัดการเตียงและทรัพยากร รวมถึงการแพทย์เฉพาะบุคคล แต่การนำไปใช้เชิงปฏิบัติจำเป็นต้องจับคู่เทคโนโลยีกับการพิสูจน์ผลลัพธ์ทางคลินิกและการกำกับดูแลที่เหมาะสม เพื่อให้เกิดความปลอดภัยและความเชื่อมั่นจากผู้ป่วยและบุคลากรด้านสุขภาพ การทำงานร่วมกันระหว่างหน่วยงานสาธารณสุข โรงพยาบาล และผู้พัฒนาแอปพลิเคชันจึงเป็นหัวใจสำคัญที่จะสร้าง governance ที่โปร่งใส กำหนดมาตรฐานข้อมูล (data standards) และวางแผนพัฒนาทักษะของบุคลากรอย่างเป็นระบบ
ในมุมมองอนาคตจนถึงปี 2034 หากมีการลงทุนเชิงยุทธศาสตร์ในข้อมูลคุณภาพสูงและการพิสูจน์ทางคลินิก (เช่น การทดลองแบบสุ่ม การศึกษาผลในสภาพแวดล้อมจริง) AI จะสามารถถูกนำมาใช้ได้อย่างยั่งยืนและวัดผลได้จริง — คาดว่าเทคโนโลยีสนับสนุนการตัดสินใจทางคลินิกอาจมีบทบาทเพิ่มขึ้นอย่างมีนัยสำคัญ (ตัวอย่างเช่น สนับสนุนการตัดสินใจใน 30–50% ของเส้นทางการดูแลบางประเภท) และช่วยลดความผิดพลาดบางรูปแบบเมื่อมีการทดสอบและกำกับอย่างเหมาะสม อย่างไรก็ตาม ความสำเร็จระยะยาวขึ้นกับการร่วมมือระหว่างภาครัฐ สถานพยาบาล และภาคเอกชนในการจัดตั้งกรอบกำกับ มาตรฐานข้อมูล โครงสร้างพื้นฐานข้อมูล และโครงการพัฒนาทักษะเพื่อให้ผลลัพธ์ที่ชัดเจนและยั่งยืนต่อระบบสุขภาพทั้งระบบ
📰 แหล่งอ้างอิง: Fortune Business Insights




